
【题目】(1)有以下四种物质:①22g二氧化碳②8g氢气③1.204×1024个氮气分子④4℃时18mL水它们所含分子数最多的是_______,所含原子数最多的______,质量最大的是_____所含电子数最多的是__________(填序号)
(2)12.4 gNa2R含Na+0.4mol,则Na2R的摩尔质量为__________,R的相对原子质量为__________,含R的质量为1.6g的Na2R,其物质的量为_____________。
【答案】② ② ③ ③ 62 g mol-1 16 0.1 mol
【解析】
(1)①22g二氧化碳,其物质的量为![]() =0.5mol;②8g氢气,其物质的量为
=0.5mol;②8g氢气,其物质的量为![]() =4mol;③1.204×1024个氮气分子,其物质的量为
=4mol;③1.204×1024个氮气分子,其物质的量为![]() =2mol,质量为2mol×28g/mol=56g;④4℃时18mL水,其质量为18mL×1g/mL=18g,物质的量为
=2mol,质量为2mol×28g/mol=56g;④4℃时18mL水,其质量为18mL×1g/mL=18g,物质的量为![]() =1mol;故所含分子数最多的是②8g氢气;
=1mol;故所含分子数最多的是②8g氢气;
①22g二氧化碳,含有原子物质的量为0.5mol×3=1.5mol;②8g氢气,含有原子物质的量为4mol×2=8mol;③1.204×1024个氮气分子,含有原子物质的量为2mol×2=4mol;④4℃时18mL水,含有原子物质的量为1mol×3=3mol;故所含原子数最多的是 ②8g氢气;
由上述计算可知,质量最大是③1.204×1024个氮气分子;
①22g二氧化碳,含有电子物质的量为0.5mol×22=11mol;②8g氢气,含有电子物质的量为4mol×2=8mol;③1.204×1024个氮气分子,含有电子物质的量为2mol×14=28mol;④4℃时18mL水,含有原子物质的量为1mol×10=10mol;故所含电子数最多的是③1.204×1024个氮气分子;
(2)1 molNa2R中含2 molNa+,题目中有Na+ 0.4mol,则有0.2 molNa2R。运用公式M=![]() 得
得![]() =62 g mol-1。然后,根据摩尔质量以g mol-1为单位时,在数值上与物质的相对原子质量或相对分子质量相等,得:Mr(Na2R) = 62,求得Mr(R) = 62-2
=62 g mol-1。然后,根据摩尔质量以g mol-1为单位时,在数值上与物质的相对原子质量或相对分子质量相等,得:Mr(Na2R) = 62,求得Mr(R) = 62-2![]() 23=16。根据n=
23=16。根据n=![]() ,得n(R) = 0.1 mol,则n(Na2R)=0.1 mol。
,得n(R) = 0.1 mol,则n(Na2R)=0.1 mol。


科目:高中化学 来源: 题型:
【题目】已知MgCl2+6NH3![]() MgCl2·6NH3该反应具有极好的可逆吸、放氨特性。某课题组在实验室探究其特性,其中氨化(吸氨)过程实验装置如图1,放氨过程实验装置如图2。
MgCl2·6NH3该反应具有极好的可逆吸、放氨特性。某课题组在实验室探究其特性,其中氨化(吸氨)过程实验装置如图1,放氨过程实验装置如图2。
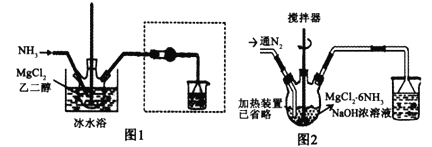
己知:相关物质的性质见下表
物质名称 | 氨气的溶解性 | 氯化镁的溶解性 | 六氨氯化镁的溶解性 |
水 | 易溶 | 易溶 | 易溶 |
甲醇(沸点65。C) | 易溶 | 易溶 | 难溶 |
乙二醇(沸点197。C) | 易溶 | 易溶 | 难溶 |
请回答:
(1)实验室采用固固加热的方式制备NH3,制备反应的方程式为___________,虚框内装置的作用是___________,氨化过程采用冰水浴的原因可能是_____(填选项序号字母)。
A.氨化过程为吸热反应,促进反应正向进行
B.加快反应速率
C.防止氨气从溶液中挥发,提高氨气利用率
D.增大六氨氯化镁的溶解度
(2)利用MgCl2溶液制备无水MgCl2,其具体操作为______________________。
(3)进行放氨实验时,三颈烧瓶加入1.97 g MgCl2·6NH3和烧碱的浓溶液,加热,并不断通入N2,通入N2目的是___________。通过观察烧杯中现象的变化就可以监控MgCl2·6NH3的放氨过程,若要判断转化率是否达到或超过90%,则烧杯中溶液可以是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着老百姓生活水平的提高,汽车进入寻常百姓家,在发生剧烈的汽车碰撞时,汽车安全气囊会发生反应10NaN3+2KNO3![]() K2O+5Na2O+16N2↑,有关该反应说法正确的是( )
K2O+5Na2O+16N2↑,有关该反应说法正确的是( )
A.氧化剂与还原剂的物质的量之比为5:1B.N2既是氧化产物也是还原产物
C.NaN3是氧化剂D.KNO3发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出。___
(2)若通入CO2气体为2.24L(标准状况下),得到9.5g的白色固体。
①请通过计算确定此白色固体组成为___。
②所用的NaOH溶液的物质的量浓度为___mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)6.02×1023个氢氧根离子的物质的量是________mol,其摩尔质量为________。
(2)3.01×1023个H2O的物质的量为________mol,其中,所有原子的物质的量为________mol,所含电子的物质的量为________mol。
(3)1.204×1023个![]() 的物质的量为________mol,质量为________g。
的物质的量为________mol,质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烧碱、纯碱等都是重要的化工原料。
(1)利用如图装置可以证明二氧化碳与烧碱溶液发生了反应。
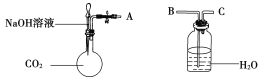
①若将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是________开始反应时的离子方程式是_______。
②若其他操作不变,将A与C连接,可观察到的现象是_______。
(2)向100mL 1mol·L-1烧碱溶液中通入一定量CO2充分反应后,将溶液在低温下蒸干得到白色固体X,X的组成可能有四种情况,按出现的先后顺序分别是Ⅰ.NaOH、Na2CO3,Ⅱ.________,Ⅲ.Na2CO3、NaHCO3,Ⅳ.________。
①常温下,将得到的固体X重新溶于水,在所得溶液中加入盐酸,使溶液的pH=7,再将溶液蒸干,得到固体的质量为________g。
②若要验证白色固体X是第Ⅰ种组成,依次加入的试剂为________(填字母序号)。
a.盐酸 b.MgCl2溶液 c.BaCl2溶液 d.Ba(OH)2溶液 e.酚酞试液
在验证的过程中,一定需要进行的操作是________(填字母序号)。
a.萃取 b.洗涤 c.过滤 d.分馏
③若白色固体X为第Ⅲ种组成,下列实验方案中不能测定其中NaHCO3质量分数的是________。
a.取m g X与足量Ba(OH)2溶液充分反应,过滤,洗涤,烘干得n g固体
b.取m g X与足量盐酸充分反应,加热,蒸干,灼烧得n g固体
c.取m g X充分加热,质量减少n g
d.取m g X与足量稀硫酸充分反应,逸出的气体被足量碱石灰吸收,增重n g
④若白色固体X的质量为7.0g,则X的组成为________(填“Ⅰ”、“Ⅱ”、“Ⅲ”或“Ⅳ”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:

已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下:Ksp[Cu(OH)2]=2.2×10-20, Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13。
回答下列问题:
(1)滤液A的主要成分除NaOH外,还有___________(填化学式);写出反应I中含铍化合物与过量盐酸反应的离子方程式:___________。
(2)滤液C中含NaCl、BeCl2和少量HCl,为得到较纯净的BeCl2溶液,选择下列实验操作最合理步骤的顺序是___________;电解熔融BeCl2制备金属铍时,需要加入NaCl,其作用是___________。
①加入过量的NaOH:②加入过量的氨水;③加入适量的HCl;④过滤;⑤洗涤。
(3)反应Ⅱ中CuS的氧化产物为S单质,该反应的化学方程式为___________。
(4)常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是________(填化学式);为了尽可能多的回收铜,所得滤液G的pH最大值为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取、净化并收集氯气涉及以下几个主要阶段:![]()
![]()
![]()
![]() 尾气处理
尾气处理
(1)写出实验室制取Cl2的离子方程式______________________,NA表示阿伏加德罗常数,若有4mol的HCl参加反应,则转移的电子总数为___________;
(2)现有以下3种试剂:A.饱和食盐水 B.浓硫酸 C.NaOH溶液
请在以上试剂中选择并回答填空:
X溶液应选用_________(填写序号);Y试剂的作用____________________.
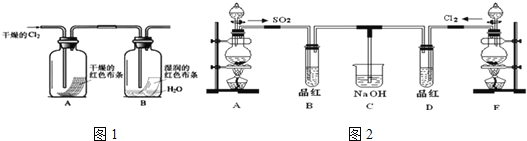
(3)某化学兴趣小组为了探究Cl2的相关性质,设计了如图1的实验.
通入Cl2后,从观察集气瓶A、B中的现象可得出的结论是_____________(写出化学反应方程式,并用简要文字解释).
(4)某兴趣小组的同学为探究和比较SO2和氯水的漂白性,设计了如图2的实验装置.
①实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:______________________;
②反应开始一段时间后,观察到B、D两试管中的品红溶液都出现褪色的现象,但两者褪色原理不同,如何区别,请你帮助设计实验,你的操作是_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下为铝土矿(主要含Fe3O4、Al2O3、SiO2)提取铝的流程,以下说法正确的是( )
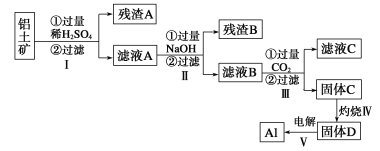
A.残渣A主要是H2SiO3B.滤液A中只存在Fe3+和Al3+
C.过程Ⅲ可以用HCl替代二氧化碳。D.滤液C主要是碳酸氢钠和硫酸钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com