
| 弱电解质 | HCOOH | HCN | H2CO3 | NH3•H2O |
| 电离平衡常数 (25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Kb=1.8×10-5 |
| A. | 由上表可知酸性HCOOH>H2CO3 | |
| B. | 0.1mol/L的HCOONH4溶液中:c(HCOO-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 0.1mol/L的NaHCO3溶液中:c(H2CO3)+c(H+)=c(OH-)+c(CO32-) | |
| D. | 结合H+的能力:CO32->HCO3->CN->HCOO- |
分析 A、HCOOH的电离度大于碳酸的第一电离度;
B、甲酸的电离程度大于氨水的电离程度,则甲酸根离子的水解程度小于铵根离子;
C、根据碳酸氢钠溶液中的电荷守恒分析;
C、相同条件下,酸的电离平衡常数越小,其越难电离,其酸根越容易结合氢离子.
解答 解:A、HCOOH的电离度大于碳酸的第一电离度,所以酸性HCOOH>H2CO3,故A正确;
B、HCOOH的电离平衡常数大于NH3•H2O,则NH4+水解程度大于HCOO-,所以HCOONH4溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒得c(HCOO-)>c(NH4+),盐溶液中氢离子浓度很小,所以离子浓度大小顺序是c(HCOO-)>c(NH4+)>c(H+)>c(OH-),故B正确;
C、碳酸氢钠溶液中存在质子守恒:c(H2CO3)+c(H+)=c(OH-)+c(CO32-),故C正确;
D、相同条件下,酸的电离平衡常数越小,其越难电离,其酸根越容易结合氢离子,所以HCOO-、CN-、HCO3-、CO32-结合质子的能力大小顺序为:CO32->CN->HCO3->HCOO-,故D错误;
故选D.
点评 本题考查了离子浓度大小比较、弱电解质的电离平衡及其影响,题目难度中等,根据电离平衡常数、酸根离子水解程度之间的关系来分析解答,灵活运用守恒思想分析是关键.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )| A. | ①②③ | B. | ①③② | C. | ②①③ | D. | ②③① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
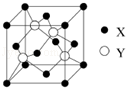 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若HAOm是强酸,则HBOm也一定为强酸 | |
| B. | 若B为非金属元素,则A可能为金属元素,若B为金属元素,则A可能为非金属元素 | |
| C. | 常温下,若B的简单氢化物是气体,则A的简单氢化物可能是液体 | |
| D. | 若B(OH)m是强碱,则A(OH)m也是强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:B>A,离子半径:C<D | |
| B. | B的单质能与A的最高价氧化物发生置换反应 | |
| C. | 元素B和D能形成BD2型的共价化合物 | |
| D. | D的单质有毒,且有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com