
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 Ni£ØCO£©4£Øg£© øĆ·“Ó¦µÄ”÷H
Ni£ØCO£©4£Øg£© øĆ·“Ó¦µÄ”÷H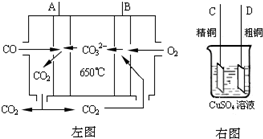
| 10 |
| 11 |
| ||
| ĒāĄė×Ó |
| ŹÆ»ŅĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014Ń§ÄźÉ½¶«Ź”ČÕÕÕŹŠøßČż3ŌĀÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
Ģ¼ŗĶµŖµÄ»ÆŗĻĪļÓėČĖĄąÉś²ś”¢Éś»īĆÜĒŠĻą¹Ų”£
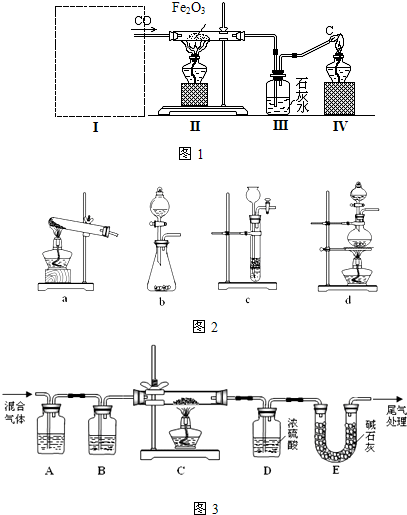
£Ø1£©ŌŚŅ»ŗćĪĀ”¢ŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ Ni(s)+4CO(g) 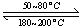 Ni(CO)4(g)£¬
Ni(CO)4(g)£¬ H<0”£ĄūÓĆøĆ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99£®9£„µÄøß“æÄų”£¶ŌøĆ·“Ó¦µÄĖµ·ØÕżČ·µÄŹĒ ?? (Ģī×ÖÄø±ąŗÅ)”£
H<0”£ĄūÓĆøĆ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99£®9£„µÄøß“æÄų”£¶ŌøĆ·“Ó¦µÄĖµ·ØÕżČ·µÄŹĒ ?? (Ģī×ÖÄø±ąŗÅ)”£
A£®Ōö¼ÓNiµÄĮææÉĢįøßCOµÄ×Ŗ»ÆĀŹ£¬NiµÄ×Ŗ»ÆĀŹ½µµĶ
B£®ĖõŠ”ČŻĘ÷ČŻ»ż£¬Ę½ŗāÓŅŅĘ£¬ H¼õŠ”
H¼õŠ”
C£®·“Ó¦“ļµ½Ę½ŗāŗ󣬳äČėCOŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬COµÄĢå»ż·ÖŹż½µµĶ
D£®µ±4v[Ni(CO)4]=v(CO)Ź±»ņČŻĘ÷ÖŠ»ģŗĻĘųĢåĆÜ¶Č²»±äŹ±£¬¶¼æÉĖµĆ÷·“Ó¦ŅŃ“ļ»ÆŃ§Ę½ŗāדĢ¬
£Ø2£©COÓėÄų·“Ó¦»įŌģ³ÉÄų“߻ƼĮÖŠ¶¾”£ĪŖ·ĄÖ¹Äų“߻ƼĮÖŠ¶¾£¬¹¤ŅµÉĻ³£ÓĆSO2½«COŃõ»Æ£¬¶žŃõ»ÆĮņ×Ŗ»ÆĪŖµ„ÖŹĮņ”£
ŅŃÖŖ£ŗC(s)+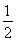 O2(g)=CO(g)??
O2(g)=CO(g)??  H=-Q1 kJ
H=-Q1 kJ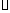 mol-1
mol-1
C(s)+ O2(g)=CO2(g)???  H=-Q2 kJ
H=-Q2 kJ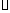 mol-1
mol-1
S(s)+O2(g)=SO2(g)????  H=-Q3 kJ
H=-Q3 kJ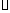 mol-1
mol-1
ŌņSO2(g)+2CO(g)=S(s)+2CO2(g)??  H=????????? ”£
H=????????? ӣ
£Ø3£©½šŹōŃõ»ÆĪļæɱ»Ņ»Ńõ»ÆĢ¼»¹ŌÉś³É½šŹōµ„ÖŹŗĶ¶žŃõ»ÆĢ¼”£Ķ¼28£Ø3£©ŹĒĖÄÖÖ½šŹōŃõ»ÆĪļ£ØCr2O3”¢SnO2”¢PbO2”¢Cu2O)±»Ņ»Ńõ»ÆĢ¼»¹ŌŹ±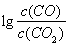 ÓėĪĀ¶Č£Øt£©µÄ¹ŲĻµĒśĻßĶ¼”£
ÓėĪĀ¶Č£Øt£©µÄ¹ŲĻµĒśĻßĶ¼”£
700oCŹ±£¬ĘäÖŠ×īÄѱ»»¹ŌµÄ½šŹōŃõ»ÆĪļŹĒ???????? (Ģī»ÆѧŹ½)£¬ÓĆŅ»Ńõ»ÆĢ¼»¹ŌøĆ½šŹōŃõ»ÆĪļŹ±£¬Čō·“Ó¦·½³ĢŹ½ĻµŹżĪŖ×ī¼ņÕūŹż±Č£¬øĆ·“Ó¦µÄĘ½ŗā³£Źż(K)ŹżÖµµČÓŚ ?????????? ”£
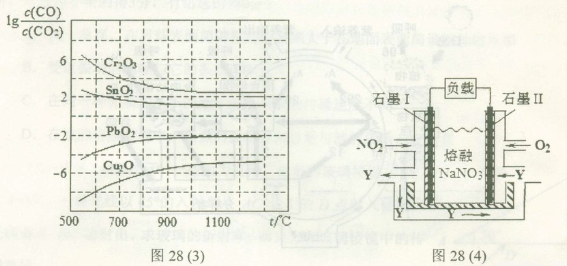
£Ø4£©NO2”¢O2ŗĶČŪČŚNaNO3æÉÖĘ×÷Č¼ĮĻµē³Ų£¬ĘäŌĄķČēÉĻĶ¼28£Ø4£©ĖłŹ¾”£øƵē³ŲŌŚŹ¹ÓĆ¹ż³ĢÖŠŹÆÄ«Iµē¼«ÉĻÉś³ÉŃõ»ÆĪļY£¬Ęäµē¼«·“Ó¦Ź½ĪŖ?????????????? ”£
ČōøĆČ¼ĮĻµē³ŲŹ¹ÓĆŅ»¶ĪŹ±¼äŗ󣬹²ŹÕ¼Æµ½20mol Y£¬ŌņĄķĀŪÉĻŠčŅŖĻūŗıź×¼×“æöĻĀŃõĘųµÄĢå»żĪŖ?? ??? L”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ¹ć¶«Ź”·šÉ½ŹŠøßČż5ŌĀĮŁæ¼¼ÆѵĄķæĘ×ŪŗĻ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
Ņ»Ńõ»ÆĢ¼ŹĒŅ»ÖÖÓĆĶ¾Ļąµ±¹ć·ŗµÄ»Æ¹¤»ł“”ŌĮĻ”£
£Ø1£©ĄūÓĆĻĀĮŠ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99.9%µÄøß“æÄų£ŗ


ŌņøĆ·“Ó¦µÄ”÷H 0£ØŃ”Ģī”°>”± »ņ”°<”±£©”£
£Ø2£©ŌŚøßĪĀĻĀŅ»Ńõ»ÆĢ¼æɽ«¶žŃõ»ÆĮņ»¹ŌĪŖµ„ÖŹĮņ”£ŅŃÖŖ£ŗ
C£Øs£©+O2(g)=CO2(g) ”÷H1=-393.5kJ.mol-1
CO2£Øg£©+C(s)=2CO(g) ”÷H2=+172.5kJ.mol-1
S£Øs£©+O2(g)=SO2(g) ”÷H3=-296.0kJ.mol-1
ĒėŠ“³öCO³żSO2µÄČČ»Æѧ·½³ĢŹ½ ”£
 £Ø3£©¹¤ŅµÉĻÓĆŅ»Ńõ»ÆĢ¼ÖĘČ”ĒāĘųµÄ·“Ó¦ĪŖ£ŗCO£Øg£©+H2O CO2(g)+H2£Øg£©£¬ŅŃÖŖ420”ꏱ£¬øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ9.0”£Čē¹ū·“Ó¦æŖŹ¼Ź±£¬ŌŚ2LµÄĆܱÕČŻĘ÷ÖŠ³äČėCOŗĶH2OµÄĪļÖŹµÄĮ涼ŹĒ0.60mol,5minÄ©“ļµ½Ę½ŗā£¬Ōņ“ĖŹ±COµÄ×Ŗ»ÆĀŹĪŖ
£¬H2µÄĘ½¾łÉś³ÉĖŁĀŹĪŖ
ӣ
£Ø3£©¹¤ŅµÉĻÓĆŅ»Ńõ»ÆĢ¼ÖĘČ”ĒāĘųµÄ·“Ó¦ĪŖ£ŗCO£Øg£©+H2O CO2(g)+H2£Øg£©£¬ŅŃÖŖ420”ꏱ£¬øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ9.0”£Čē¹ū·“Ó¦æŖŹ¼Ź±£¬ŌŚ2LµÄĆܱÕČŻĘ÷ÖŠ³äČėCOŗĶH2OµÄĪļÖŹµÄĮ涼ŹĒ0.60mol,5minÄ©“ļµ½Ę½ŗā£¬Ōņ“ĖŹ±COµÄ×Ŗ»ÆĀŹĪŖ
£¬H2µÄĘ½¾łÉś³ÉĖŁĀŹĪŖ
ӣ
£Ø4£©ĻĀĶ¼ÖŠĶ¼1ŹĒŅ»ÖÖŠĀŠĶČ¼ĮĻµē³Ų£¬ĖüŅŌCOĪŖČ¼ĮĻ£¬Ņ»¶Ø±ČĄżµÄLi2CO3ŗĶNa2CO3ČŪČŚ»ģŗĻĪļĪŖµē½āÖŹ£¬Ķ¼2ŹĒ“ÖĶ¾«Į¶µÄ×°ÖĆĶ¼£¬ĻÖÓĆČ¼ĮĻµē³ŲĪŖµēŌ“½ųŠŠ“ÖĶµÄ¾«Į¶ŹµŃ锣
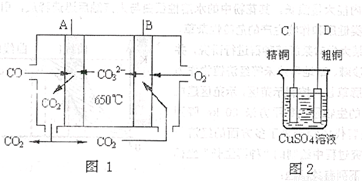
»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁŠ“³öA¼«·¢ÉśµÄµē¼«·“Ó¦Ź½ ”£
¢ŚŅŖÓĆČ¼ĮĻµē³ŲĪŖµēŌ“½ųŠŠ“ÖĶµÄ¾«Į¶ŹµŃ飬ŌņB¼«Ó¦øĆÓė ¼«£ØĢī”°C”±»ņ”°D”±£©ĻąĮ¬”£
¢Ūµ±Ļūŗıź×¼×“æöĻĀ2.24LCOŹ±£¬Cµē¼«µÄÖŹĮæ±ä»ÆĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com