
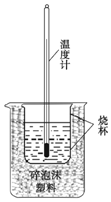
 ʵ����������ͼװ�ý����к��ȵIJⶨ�� �ش��������⣺
ʵ����������ͼװ�ý����к��ȵIJⶨ�� �ش��������⣺| ��Ӧ�� | ��ʼ�¶ȣ��棩 | �����¶ȣ��棩 | �к��ȣ�kJ•mol-1�� |
| ��HCl+NaOH | 13 | 19.8 | -a |
| ��HCl+NH3•H2O | 13 | 19.3 | -b |
���� ��1���������ȼƵĹ������жϸ�װ�õ�ȱ�������������к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�����
��2������������ʵ�����Ҫ����������Ϊ��ʹ�����ַ�Ӧ����ҺӦ�������ȸ���Q=m•c•��T���㷴Ӧ�ų���������Ȼ����ݡ�H=-$\frac{Q}{n}$kJ/mol�������Ӧ�ȣ�
��� �⣺��1�������ȼƵĹ����֪��װ�õ�ȱ�������ǻ��β����������Ϊ�˼�����������ʧ���ձ��Ϸ���Ӳֽ�壻
�ʴ�Ϊ�����β�����������ձ��Ϸ���Ӳֽ�壻
��2��NH3•H2O�������Ϊ�к����з�������Ҫ���ȣ�������Ƚ��٣��к�����ֵƫС������a��b��
��Һ������Ŀ����ʹ�����ַ�Ӧ�����ʵ���ȷ�ȣ�
50mL1.0mol•L-1��������50mL 1.1mol•L-1�� NaOH��Һ�����кͷ�Ӧ����ˮ�����ʵ���Ϊ0.05L��1.0mol•L-1=0.05mol����Һ������Ϊ��100ml��1g/ml=100g���¶ȱ仯��ֵΪ6.8�棬������0.05molˮ�ų�������ΪQ=m•c•��T=100g��4.18J/��g•�棩��6.8��=2842.4kJ������ʵ���õ��к��ȡ�H=-$\frac{2842.4kJ}{0.05mol}$=-56.8 kJ/mol��
�ʴ�Ϊ������ʹ�����ַ�Ӧ�����ʵ���ȷ�ȣ�56.8��
���� ���⿼�����к��ȵIJⶨ����ȷ�к��ȵĶ���Ͳ����к��ȵ�ԭ���ǽ���ؼ���ע��ʵ����������йؼ����ھ����ܼ�������ɢʧ���ⶨ�������ȷ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ࡢ���ס����� | B�� | ���ܲ���ˮ�������� | ||
| C�� | �⡢������ | D�� | �����߲ˡ������ס��ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ԭ����ͭ����Ӧ��ɺ���ֹͣͨ������ֹͣ���� | |
| B�� | ������FeCl3��Һ����������Ʊ�Fe��OH3���壩 | |
| C�� | ��ҵ�Ʊ�HCl����ʱ�������������Ļ�������ڹ��������·�Ӧ | |
| D�� | Ũ����ϡ��ʱ��ͼ���� |
�鿴�𰸺ͽ���>>
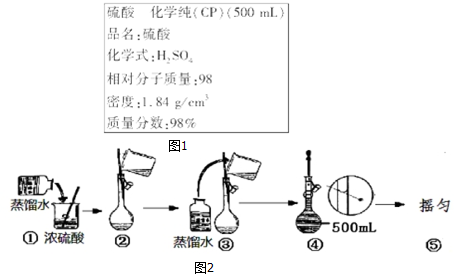
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��Ϊͬ���칹�� ��Ϊͬ���칹�� | |
| B�� |  �� ��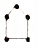 ��������Ϊͬϵ�� ��������Ϊͬϵ�� | |
| C�� | �ױ����������ķ�Ӧ�����ܷ�Ӧ������Ӱ�����ͬ | |
| D�� | H2��D2��Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2 | B�� | HCl | C�� | O2 | D�� | CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ�У�Na+��Cl-��SO42-��Cu2+ | |
| B�� | �μ���ɫʯ����Һ�Ժ�ɫ����Һ��NH4+��Fe2+��SO42-��NO3- | |
| C�� | �μӷ�̪�Ժ�ɫ����Һ��K+��Ba2+��Cl-��NO32- | |
| D�� | ���д���HS-����Һ��NH4+��Ca2+��H+��I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 44g CO2���е�ԭ����ĿΪ NA | |
| B�� | 1L1 mol•L-1 �ģ�NH4��2SO4 ��Һ�к��е� NH4+��ĿΪ2NA | |
| C�� | ������ MnO2�� 100mL12 mol•L-1��Ũ�����ַ�Ӧ��ת�Ƶĵ�����ĿΪ 0.6 NA | |
| D�� | ���³�ѹ�£�18mL ˮ���еķ�����ĿԼΪ NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com