
分析 (1)根据物质具有的能量进行计算:△H=E(生成物的总能量)-E(反应物的总能量),当反应物的总能量大于生成物的总能量时,反应放热,当反应物的总能量小于生成物的总能量时,反应吸热;
(2)3H2+N2?2NH3,依据反应焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量计算得到.
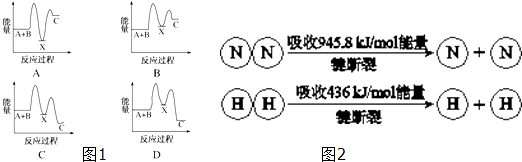
解答 解:(1)A+B→C为放热反应,则A+B的总能量大于生成C的总能量,排除选项A、B,A+B→X(吸热),则X的能量大于A+B的总能量,X→C(放热),则X的能量大于C的总能量,排除选项C,
故选D;
(2)工业合成氨反应为:3H2+N2?2NH3,反应焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量=3×436+945.8-6×N-H键键能=-92.2,N-H键键能=+391kJ,
故答案为:391.
点评 本题为图象题,主要考查了物质的能量分析应用,化学反应的能量变化、分析,题目难度不大,注意反应热与物质总能量大小的关系判断.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{19}^{40}K$与${\;}_{20}^{40}Ca$ | B. | D2O与T2O | ||
| C. | ${\;}_{19}^{40}K$与${\;}_{19}^{39}K$ | D. | 白磷与红磷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为甲醇分子中不含有碳碳双键,所以甲醇不能使酸性高锰酸钾溶液褪色 | |
| B. | 甲苯不使溴水褪色,但甲苯和溴可以发生取代反应 | |
| C. | 乙烯在一定条件下与氧气反应生成乙醛,乙烯发生了氧化反应 | |
| D. | 蛋氨酸分子中含有羧基(-COOH)和氨基(-NH2) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
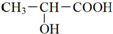 .在多种生物化学过程中乳酸起重要作用,在一般的新陈代谢和运动中乳酸不断被产生.请回答下列问题:
.在多种生物化学过程中乳酸起重要作用,在一般的新陈代谢和运动中乳酸不断被产生.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com