
【题目】利用海洋资源获得的部分物质如图所示.下列说法正确的是( )
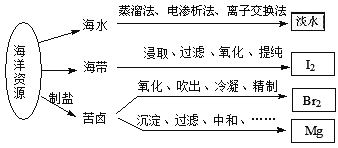
A. 从海水中获取淡水,历史最久的方法是离子交换法
B. 实验室中从海带中获得I2,需要用到的主要仪器有蒸发皿、漏斗、烧杯、分液漏斗等
C. 用SO2溶液吸收从苦卤中吹出的单质溴时,发生的离子反应是Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
D. 用石灰石、盐酸等从苦卤中提取镁时,发生反应的反应类型有化合、分解、置换和复分解
【答案】C
【解析】试题分析:A.从海水中获取淡水历史最悠久的方法是蒸馏,故A错误;B.提取海带中的碘元素不需要溶液蒸发,不需要蒸发皿,故B错误;C.用SO2溶液吸收从苦卤中吹出的单质溴时,利用二氧化硫还原性和溴单质发生氧化还原反应生成溴化氢和硫酸,发生的离子反应是Br2+SO2+2H2O═4H++SO42-+2Br-,故C正确;D.海水提取镁单质的过程中发生的反应有:CaCO3![]() CaO+CO2↑、CaO+H2O=Ca(OH)2、Mg2++2OH-=Mg(OH)2↓、Mg(OH)2+2HCl=MgCl2+2H2O、MgCl2(熔融)
CaO+CO2↑、CaO+H2O=Ca(OH)2、Mg2++2OH-=Mg(OH)2↓、Mg(OH)2+2HCl=MgCl2+2H2O、MgCl2(熔融)![]() Mg+Cl2↑,所以涉及的反应有化合反应、复分解反应和分解反应,不涉及置换反应,故D错误;故选C。
Mg+Cl2↑,所以涉及的反应有化合反应、复分解反应和分解反应,不涉及置换反应,故D错误;故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】右图是373K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 ( )
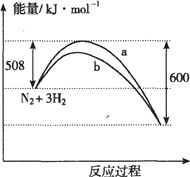
A. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92kJ·mol-1
2NH3 △H=-92kJ·mol-1
B. 加入催化剂,该化学反应的反应热不变
C. a曲线是加入催化剂时的能量变化曲线
D. 在温度体积一定的条件下,通入1mol N2和3 mol H2反应后放出的热量为Q1kJ,则Q1=92
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下:

已知:AlCl3·6H2O易溶于水、乙醇及乙醚;明矾在水中的溶解度如下表。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
请回答:
(1)步骤Ⅰ中的化学方程式_________;步骤Ⅱ中生成Al(OH)3的离子方程式___________。
(2)步骤Ⅲ,下列操作合理的是____________。
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序_______________。
①迅速降至室温 ②用玻璃棒摩擦器壁 ③配制90℃的明矾饱和溶液 ④自然冷却至室温 ⑤选规则明矾小晶体并悬挂在溶液中央 ⑥配制高于室温10-20℃的明矾饱和溶液
(4)由溶液A制备AlCl3·6H2O的装置如下图:

①通入HCl的作用是抑制AlCl3水解和________________________。
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是_____;洗涤时,合适的洗涤剂是_____。
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途不对应的是( )
A. 铝合金的密度小,硬度大,可用作建筑材料
B. 食品工业中用Na2CO3作焙制糕点的膨松剂
C. FeCl3溶液能与Cu反应,可用于腐蚀铜制印刷电路板
D. 明矾能生成Al(OH)3胶体,可用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
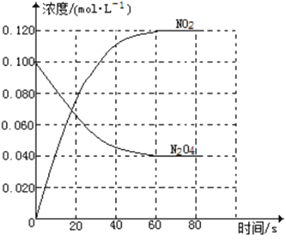
【题目】(1)在容积为1.00L的容器中,通入一定量的N2O4发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
①反应的△H_______0(填“大于”“小于”);
②100℃时,体系中各物质浓度随时间变化如右图所示。在0~60s时段,反应速率v(N2O4)为_________molL-1s-1反应的平衡常数K为__________。
(2)在恒容密闭容器中通入X 并发生反应:2X(g) = Y(g);温度T1、T2下X的物质的最浓度c(X)随时间t 变化的曲线如图所示。
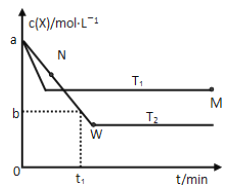
①T1____T2 (填“大于”或“小于”)。
②M点的正反应速率V正____N点的逆反应速率V逆(填“大于”,“小于”或“等于”)。
(3)CuBr2分解的热化学方程式为:2CuBr2(s)=2CuBr(s) + Br2(g) ΔH= + 105. 4kJ/mol。在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会_______(填“增大”、“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(l)基态As原子的核外电子排布式为[Ar]______,有________个未成对电子。
(2) As与N是同主族元素,从原子结构角度分析:为什么As的最高价含氧酸H3AsO4是三元酸(含三个轻基),而N的最高价含氧酸HNO3是一元酸(只含一个烃基)______。
(3)比较下列氢化物的熔点和沸点,分析其变化规律及原因__________。
(4) Na3AsO3中Na、As、O电负性由大至小的顺序是______。AsO33-的空间构型为___, AsO33-中As的杂化轨道类型为_______杂化。
(5)砷化稼(GaAs)为黑灰色固体,熔点为1238℃。该晶体属于___晶体,微粒之间存在的作用力是_________。
NH3 | PH3 | AsH3 | SbH3 | |
熔点/K | 195.3 | 140.5 | 156.1 | 185 |
沸点/K | 239.6 | 185.6 | 210.5 | 254.6 |
(6)图为GaAs的晶胞,原子半径相对大小是符合事实的,则白球代表____原子。
己知GaAs的密度为5.307g·cm3, Ga和As的相对原子质量分别为69.72、74.92,求晶胞参数a=______pm (列出计算式即可)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com