
����Ŀ����ϩ�棨CH2=CHCN����һ����Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ��á���ϩ������������������Ҫ�������б�ϩȩ��CH2=CHCHO�������棨CH3CN���ȣ��ش��������⣺
��1���Ա�ϩ����������Ϊԭ�ϣ��ڴ������������ɱ�ϩ�棨C3H3N���������ϩȩ��C3H4O�����Ȼ�ѧ����ʽ���£�
C3H6��g��+NH3��g��+ ![]() O2��g��=C3H3N��g��+3H2O��g����H=��515kJ/mol
O2��g��=C3H3N��g��+3H2O��g����H=��515kJ/mol
C3H6��g��+O2��g��=C3H4O��g��+H2O��g����H=��353kJ/mol
������Ӧ������ѧ�����ƾ��ܴ���ԭ��������������߱�ϩ��ƽ����ʵķ�Ӧ����������߱�ϩ�淴Ӧѡ���ԵĹؼ������� ��
��2��ͼ��a��Ϊ��ϩ������뷴Ӧ�¶ȵĹ�ϵ���ߣ���߲��ʶ�Ӧ�¶�Ϊ460�森����460��ʱ����ϩ��IJ�������ǡ����ߡ����ǡ�����Ӧ�¶��µ�ƽ��
���ʣ��ж�������������460��ʱ����ϩ����ʽ��͵Ŀ���ԭ������˫ѡ�����ţ�
A���������Խ��� B��ƽ�ⳣ����� C������Ӧ���� D����Ӧ�������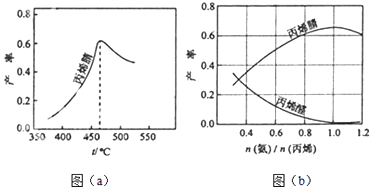
��3����ϩ��ͱ�ϩȩ�IJ�����n������/n����ϩ���Ĺ�ϵ��ͼ��b����ʾ����ͼ��֪�����n������/n����ϩ��ԼΪ �� ������ �� ������������������ϩ�����������ԼΪ
���𰸡�
��1��������Ӧ��Ϊ��������ķ�Ӧ�����¡���ѹ������
��2�����ǣ��÷�ӦΪ���ȷ�Ӧ��ƽ�����Ӧ���¶����߶����ͣ�AC
��3��1��1���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ�1��7.5��1
���������⣺��1��������Ӧ������ѧ�����ƾ��ܴ�������Ӧ������������Ӧ������������������������ѧ���ƴ÷�ӦΪ�����������ķ��ȷ�Ӧ�����Խ����¶ȡ�����ѹǿ��������߱�ϩ���ƽ����ʣ���߱�ϩ�淴Ӧѡ���ԵĹؼ������Ǵ�����
���Դ��ǣ�������Ӧ��Ϊ��������ķ�Ӧ�����¡���ѹ����������2����Ϊ�÷�ӦΪ���ȷ�Ӧ��ƽ�����Ӧ���¶����߶����ͣ�������460��ʱ����Ӧ�¶��µ�ƽ��ת��������Ӧ�����½��ģ���ʵ�������������ģ�����жϵ���460��ʱ����ϩ��IJ��ʲ��Ƕ�Ӧ�¶��µ�ƽ��ת���ʣ�����460��Cʱ����ϩ����ʽ��ͣ�
A��������һ���¶ȷ�Χ�ڻ��Խϸߣ����¶ȹ��ߣ����Խ��ͣ���A��ȷ��
B����ͼ���֪�������¶�ƽ�ⳣ����С����B����
C���������⣬�������б�ϩȩ���������Խ��ͣ�����Ӧ���࣬���²����½�����C��ȷ��
D����Ӧ��ܵĴ�С��Ӱ��ƽ�⣬��D����
���Դ��ǣ����ǣ��÷�ӦΪ���ȷ�Ӧ��ƽ�����Ӧ���¶����߶����ͣ�AC����3������ͼ���֪���� ![]() ԼΪ1ʱ���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ����ݻ�ѧ��ӦC3H6��g��+NH3��g��+
ԼΪ1ʱ���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ����ݻ�ѧ��ӦC3H6��g��+NH3��g��+ ![]() O2��g��=C3H3N��g��+3H2O��g������������������ϩ��1��1.5��1������ȼ��뷴Ӧ�ﵽ���״̬��������������Լռ20%�����Խ��ϰ�����������ϩ���������ԼΪ��1��7.5��1��
O2��g��=C3H3N��g��+3H2O��g������������������ϩ��1��1.5��1������ȼ��뷴Ӧ�ﵽ���״̬��������������Լռ20%�����Խ��ϰ�����������ϩ���������ԼΪ��1��7.5��1��
���Դ��ǣ�1��1���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ�1��7.5��1��
�����㾫�������ڱ��⿼��Ļ�ѧƽ��״̬���ʼ���������Ҫ�˽⻯ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч�����ܵó���ȷ�𰸣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ���˵����ȷ���ǣ� ��
A.��pH��ֽ��˫��ˮ��pH
B.����ʽ�ζ�����ȡ20.00 mL����K2Cr2O7��Һ
C.��������ƽ��ȡ 5.85 g NaCl����
D.�ô�ĥ�ڲ��������Լ�ƿ����Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС����Ƶ�ⱥ��ʳ��ˮ��װ����ͼ��ͨ��������������ݲ�������Һ������������������ȷ���ǣ� �� 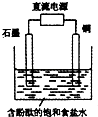
A.ͭ�缫�Ϸ�����ԭ��Ӧ
B.ʯī�缫������Һ�ʺ�ɫ
C.��Һ�е�Na+��ʯī�缫�ƶ�
D.ͭ�缫�����۲쵽����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ���������PFS����ˮ��������Ҫ������������ͼ���Ի��շ���мΪԭ���Ʊ�PFS��һ�ֹ������̣� 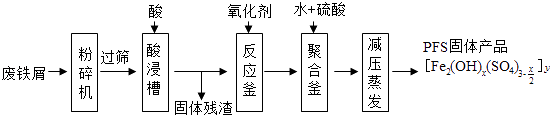
�ش���������
��1������м��ҪΪ���渽�д�������������������Ҫ�ɷ�Ϊ �� �����ɸ��Ŀ���� ��
��2�����ʱ����ʵ����� �� д���������ᷴӦ�����ӷ���ʽ ��
��3����Ӧ���м����������������� �� ����������������ʵ��������ţ���
A��KMnO4 B��Cl2 C��H2O2 D��HNO3
��4���ۺϸ�����Һ��pH���������һ���ķ�Χ�ڣ�pHƫСʱFe3+ˮ��̶�����pHƫ��ʱ�� ��
��5������ڳ�ѹ��������ѹ�������ŵ��� ��
��6���λ���B�Ǻ�������������Ч������Ҫָ�꣬����ʽΪB= ![]() ��nΪ���ʵ�������Ϊ������Ʒ��Bֵ��ȡ��Ʒm g��ȷ����������ᣬ��ַ�Ӧ���ټ�����к���ȴ������ˮ���Է�̪Ϊָʾ������c molL��1�ı�NaOH��Һ�����к͵ζ������ֲ�����ȥ�����ų������Ӹ��ţ������յ�ʱ����NaOH��ҺV mL���������������հ������飬����NaOH��ҺV0 mL����֪����Ʒ��Fe����������w����B�ı���ʽΪ ��
��nΪ���ʵ�������Ϊ������Ʒ��Bֵ��ȡ��Ʒm g��ȷ����������ᣬ��ַ�Ӧ���ټ�����к���ȴ������ˮ���Է�̪Ϊָʾ������c molL��1�ı�NaOH��Һ�����к͵ζ������ֲ�����ȥ�����ų������Ӹ��ţ������յ�ʱ����NaOH��ҺV mL���������������հ������飬����NaOH��ҺV0 mL����֪����Ʒ��Fe����������w����B�ı���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ��Ӧ���ʵ���Ҫ�����ǣ�������
A. �μӷ�Ӧ�ﱾ��������B. ����
C. �¶Ⱥ�ѹǿ�Լ���Ӧ��ĽӴ���D. ��Ӧ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǹ�ˮ����{[Cr��CH3COO��2]22H2O����Է�������Ϊ376}��һ�����ɫ���壬��������ˮ���dz��õ��������ռ���ʵ��������п�������Ȼ�����Һ����������Һ������Ϊ��Ҫԭ���Ʊ������Ǹ�ˮ�����װ����ͼ��ʾ��������2��Ԥ�ȼ���п������֪���۸����ȶ������ױ���������������п��Ӧ���Ʊ������з�������ط�Ӧ���£�
Zn��s��+2HCl��aq���TZnCl2��aq��+H2��g��
2CrCl3��aq��+Zn��s���T2CrCl2��aq��+ZnCl2��aq��
2Cr2+��aq��+4CH3COO����aq��+2H2O��l���T[Cr��CH3COO��2]22H2O��s��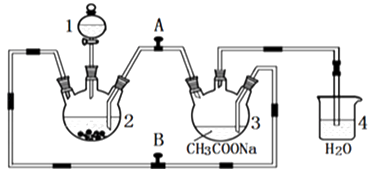
��ش��������⣺
��1������1�������� ��
��2��������2�м���������Ȼ�����Һ��˳���������ѡ�����A��B��C����Ŀ���� ��
A����������Ȼ�����Һͬʱ���� B���ȼ����Ȼ�����Һһ��ʱ����ټ�����C���ȼ�����һ��ʱ����ټ����Ȼ�����Һ
��3��Ϊʹ���ɵ�CrCl2��Һ��CH3COONa��Һ˳����ϣ�Ӧ�رշ������A����B������ͬ�������� ��
��4����ʵ����п��Ҫ��������ԭ������ò�����H2��CrCl2��Һѹ��װ��3��CH3COONa��Һ��Ӧ�⣬��һ�������� ��
��5����֪������Ӧ��������ʵ��ʱȡ�õ�CrCl3��Һ�к�����9.51g��ȡ�õĴ�������ҺΪ1.5L0.1mol/L��ʵ���ø��﴿����[Cr��CH3COO��2]22H2O9.4g�����ʵ�����ò�Ʒ�IJ���Ϊ���������ܽ�Ĵ����Ǹ�ˮ�����
��6���������ӻ���Ⱦˮ��������Ҫ��ȥ����ʵ���ж����Cr2+ �� �������Һ��ͨ�������ģ��ټ����Һ������pH����Ϊ����ʹ�������ӳ�����ȫ����������Ũ��ӦС��10��5mol/L��������֪Cr��OH��3���ܶȻ�Ϊ6.3��10��31 �� ![]() ��4��lg2��0.3��
��4��lg2��0.3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������ͱ���FeBr3������ȡ�屽���õ����屽��Ҫ�����²����ᴿ����1������2��ˮϴ����3���ø���������4����10%��NaOH��Һϴ�ӣ���ȷ�IJ���˳���ǣ� ��
A.��1����2����3����4��
B.��4����2����3����1��
C.��4����1����2����3��
D.��2����4����2����3����1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.������ѧ��Ӧʱʧȥ����Խ��Ľ���ԭ�ӣ���ԭ����Խǿ
B.���������ӱ���ԭ��һ���õ���Ԫ�صĵ���
C.�������������ͬ��ԭ�ӣ�һ����ͬ��Ԫ�ص�ԭ��
D.��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������������H+��Cl����Fe3+��ͬһ��Һ�д����������
A.Fe2+B.ClO��C.I��D.HCO3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com