
生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12 000~20 000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
| N≡N | F—F | N—F | |
| 1 mol分子中的化学键断裂 时需要吸收的能量/kJ | 941.7 | 154.8 | 283.0 |
下列说法中正确的是
A.过程N2(g)―→2N(g)放出能量
B.过程N(g)+3F(g)―→NF3(g)放出能量
C.反应N2(g)+3F2(g)―→2NF3(g)的ΔH>0
D.NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
科目:高中化学 来源: 题型:
X、Y、Z、R为前四周期元素且原子序数依次增大。X的单质与氢气可以化合生成气体G,其水溶液pH>7;Y单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。Y、Z分别与钠元素可以形成化合物Q和J ,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M。
,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M。
请回答下列问题:
⑴M固体的晶体类型是 。
⑵Y基态原子的核外电子排布式是 ① ;G分子中X原子的杂化轨道的类型是 ② 。
⑶L的悬浊液加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是 。
⑷R的一种含氧酸根RO42-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。请回答下列问题:
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃烧热____(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的气化热为44 kJ/mol,则表示氢气燃烧热的热化学方程式为______________________________。
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃)

该反应为_________反应(填“放热”或“吸热”);在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)
ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)
ΔH2=-1 160 kJ·mol-1
若在标准状况下用CH4还原4.48 L NO2气体至N2,则下列说法中正确的是
A.该过程吸收的热量为86.7 kJ
B.此过程中需要CH4气体1.12 L
C.转移的电子数为0.8NA个
D.已知2NO(g)+O2(g)===2NO2(g) ΔH=-114 kJ·mol-1,则CH4的燃烧热是802 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A(g)+3B(g)  2C(g) ΔH=-Q kJ·mol-1。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2。下列叙述不正确的是
2C(g) ΔH=-Q kJ·mol-1。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2。下列叙述不正确的是
A.甲中A的转化率为75%
B.Q1+Q2=Q
C.达到平衡后,再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向正向移动
D.乙中的热化学方程式为2C(g)  A(g)+3B(g) ΔH=+Q2 kJ·mol-1
A(g)+3B(g) ΔH=+Q2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
| 化学方程式 | 焓变ΔH (kJ·mol-1) | |
| 甲烷 氧化 | CH4(g)+2O2(g)===CO2(g)+2H2O(g) | ΔH1 |
| CH4(g)+O2(g)===CO2(g)+2H2(g) | -322.0 | |
| 蒸汽 重整 | CH4(g)+H2O(g)===CO(g)+3H2(g) | 206.2 |
| CH4(g)+2H2O(g)===CO2(g)+4H2(g) | 165.0 |
①反应CO(g)+H2O(g)===CO2(g)+H2(g)的ΔH=________ kJ·mol-1。
②甲烷的燃烧热为ΔH2,则ΔH2________ΔH1(填“>”、“=”或“<”)。
(2)物质(tBuNO)2在正庚烷溶剂中发生如下反应:
(tBuNO)22(tBuNO) ΔH。
实验测得该反应的ΔH=+50.5 kJ·mol-1,活化能Ea=90.4 kJ·mol-1。下列能量关系图合理的是________________________________________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列选项中最后的物质是要制取的物质,其中不可能得到的是( )
A.CaCO3 CaO
CaO Ca(OH)2
Ca(OH)2 NaOH溶液
NaOH溶液
B.Cu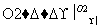 CuO
CuO CuSO4溶液
CuSO4溶液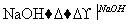 Cu(OH)2沉淀
Cu(OH)2沉淀
C.KMnO4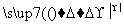 O2
O2 SO3
SO3 H2SO4溶液
H2SO4溶液
D.BaCO3 BaCl2溶液
BaCl2溶液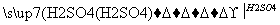 BaSO4沉淀
BaSO4沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
 柠檬中含有大量的柠檬酸,因此被誉为“柠檬酸仓库”。柠檬酸的结构简式为
柠檬中含有大量的柠檬酸,因此被誉为“柠檬酸仓库”。柠檬酸的结构简式为 ,
,
则1 mol柠檬酸与足量的金属钠反应,最多可消耗Na的物质的量为( )
A.2 mol B.3 mol
C.4 mol D.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列反应中,水仅作还原剂的是( )
A.Na2O+H2O=2NaOH B.2F2+2H2O=4HF+O2[
C.Cl2+H2O=HCl+HClO D.2K+2H2O=2KOH+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com