
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
| 第三次 | 10.00 | 0.40 | 23.40 |
| C(标准)×V(标准) |
| V(待测) |
| C(标准)×V(标准) |
| V(待测) |
| C(标准)×V(标准) |
| V(待测) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、9gD2O所含有的质子数为5NA |
| B、100mL1mol?L-1AlCl3溶液中含的阳离子数大于0.1NA |
| C、25℃时,pH=12的1.0 L NaClO溶液中水电离出的OH-的数目为0.01 NA |
| D、7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
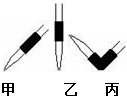 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 23.54 | 20.00 |
| 2 | 0.10 | 23.96 | 20.00 |
| 3 | 0.10 | 24.00 | 20.00 |
| 4 | 0.10 | 24.04 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
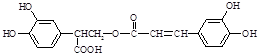
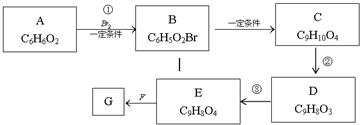
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ |
| C、NaHCO3溶液和过量Ba(OH)2溶液混合:2HCO3-+2OH-+Ba2+═BaCO3↓+2H2O+CO32- |
| D、NaAlO2溶液中通入少量CO2:2A1O2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
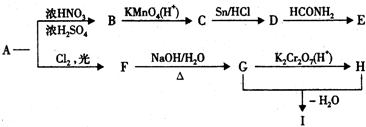
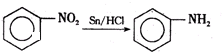

 ,物质E含2个六元环.
,物质E含2个六元环.查看答案和解析>>
科目:高中化学 来源: 题型:
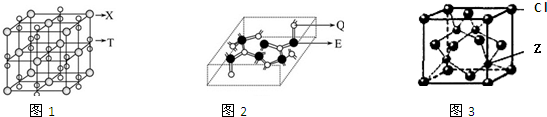
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①③ |
| C、②④ | D、其它组合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com