
(1)甲醇(CH3OH)是重要的能源物质,研究甲醇具有重要意义。为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-。电池工作时正极反应式为 。
若以该电池为电源,用石墨做电极电解100 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/mol·L-1 | 1 | 4 | 4 | 1 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上收集到氧气标况下的体积为 L。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用右图装置模拟上述过程:
①写出阳极电极反应式 ;
②除去甲醇的离子反应为 ,该过程中被氧化的元素是_____ ,当产生标准状况下2.24 L CO2时,共转移电子 mol。
科目:高中化学 来源:2015-2016学年浙江省桐乡市高二上期中(普通班)化学试卷(解析版) 题型:选择题
用惰性电极分别电解下列各电解质的水溶液,一段时间后(设电解质足量),向电解后溶液中加入适量原电解质,可以使溶液恢复到电解前的浓度的是
A.Cu(NO3)2 B.K2SO4 C.HCl D.NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省高一上段考化学试卷(解析版) 题型:选择题
在标准状况下①6.72L CH4 ②3.01×1023个HCl分子③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
A.物质的量②>③>①>④ B.体积②>③>①>④
C.质量②>③>①>④ D.氢原子个数②>③>①>④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期末化学试卷(解析版) 题型:选择题
在0.1 mol·L-1的NaHCO3溶液中,下列关系式错误的是( )
A.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
B.c(Na+)> c(HCO3-)>c(OH-)>c(H2CO3)> c(CO32-)
C.c(Na+)+c(H+)= c(HCO3-)+2 c(CO32-)+c(OH-)
D.c(Na+)=c(H2CO3)+ c(HCO3-)+ c(CO32-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期末化学试卷(解析版) 题型:选择题
下列化学方程式中,属于水解反应的是( )。
A.H2O+H2O=H3O++OH- B.HCO3-+OH-=H2O+CO32-
C.CO2+H2O=H2CO3 D.CO32-+H2O=HCO3-+OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末考试化学试卷(解析版) 题型:选择题
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)  2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如表所示:
2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如表所示:
容器 编号 | 起始时各物质的物质的量/mol | 达到平衡时体 系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出能量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是( )
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为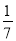
C.容器②中达到平衡时放出的热量Q=23.15 kJ
D.若容器①体积为0.5 L,则平衡时放出的热量<23.15 kJ
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末考试化学试卷(解析版) 题型:选择题
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2恰好恢复到电解前的浓度和pH.则电解过程中转移电子的总物质的量为( )
A.0.2mol B.0.4mol C.0.6mol D.0.8mol
查看答案和解析>>
科目:高中化学 来源:2015-2016年陕西西藏民族学院附属中学高二上期末化学卷(解析版) 题型:填空题
已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
请回答下列问题:
(1)写出上述反应的化学方程式 .
(2)该反应的正反应是 反应(填“放热”或者“吸热”)
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:

①此时系统温度400℃,比较正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”).
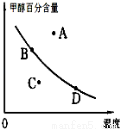
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中 点.比较图中B、D两点所对应的正反应速率B D(填“>”、“<”或 “=”).理由是 .
(4)一定条件下要提高反应物的转化率,可以采用的措施是
a.升高温度 b.加入催化剂
c.压缩容器的体积 d.增加水蒸气的浓度
e.及时分离出产物.
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第四次月考理综化学试卷(解析版) 题型:选择题
下列物质中均含有酸性杂质,除去这些杂质的方法中正确的是
A.乙醇中含乙酸杂质:加入足量氧化钙,蒸馏
B.制氯气时,依次通过饱和NaHCO3溶液和浓硫酸净化气体
C.CO2中混有H2S通过足量的浓硫酸溶液洗气,以得到纯净的CO2
D.通过灼热的镁粉除去N2中的O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com