
 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中,试回答下列问题:
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中,试回答下列问题:

科目:高中化学 来源: 题型:
| A、在卤代烃中直接加入AgNO3溶液 |
| B、加蒸馏水,充分搅拌后,加入AgNO3溶液 |
| C、加入NaOH溶液,加热后加入稀硝酸酸化,再加入AgNO3溶液 |
| D、加入NaOH的乙醇溶液,加热后加入AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
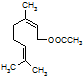 乙酸橙花酯是一种食用香料,结构如图所示.下列关于该物质的说法有:
乙酸橙花酯是一种食用香料,结构如图所示.下列关于该物质的说法有:| A、①③④ | B、②③⑤ |
| C、①④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、950 mL;111.2 g |
| B、1000 mL;117 g |
| C、500 mL;117 g |
| D、1000 mL;111.2 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Ba2+)=c(SO42-)=( Ksp) |
| B、c(Ba2+)?c(SO42-)>Ksp,c(Ba2+)=c(SO42-) |
| C、c(Ba2+)?c(SO42-)=Ksp,c(Ba2+)>c(SO42-) |
| D、c(Ba2+)?c(SO42-)≠Ksp,c(Ba2+)<c(SO42-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com