
| 9 |
| 4 |
| ������ |
| ��ʼ�� |
| x2 |
| (2-x)2 |
| 9 |
| 4 |
| ������ |
| ��ʼ�� |
| 1.2mol/L |
| 2mol/L |
| 1��1 |
| 1��1 |
| (1+y)2 |
| (1-y)2 |
| 9 |
| 4 |
| 2��2 |
| 2��2 |


 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
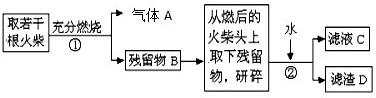
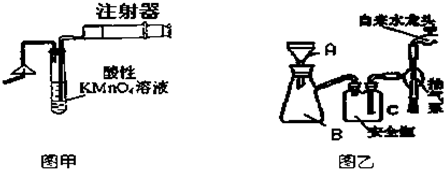
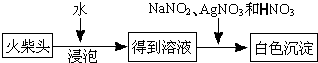
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
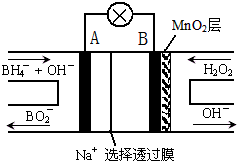
| A���缫BΪ���� |
| B���ŵ�����У�Na+������������Ǩ�� |
| C����ظ����ĵ缫��ӦΪ��BH4-+8OH--8e-�TBO2-+6H2O |
| D���ڵ�ط�Ӧ�У�ÿ����1L 6mol/L H2O2��Һ��������������·�еĵ���Ϊ12NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ba2+ | Cu2+ | Ag+ | |
| Cl- | �� | �� | �� |
| CO | �� | �� | �� |
| SO | �� | �� | |
| S2- | �� | �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����NaH����ˮ���õ���ˮ��Һ�ܵ���˵��NaH�����ӻ����� |
| B��Fe��OH��3�����Fe��OH��3�����Ļ�ѧ���ʲ���ͬ |
| C���Ҵ������к��ǻ�����������Ʒ�Ӧ�������� |
| D��MnO2���н�ǿ�����ԣ�����ΪH2O2�ֽⷴӦ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�����Һ�У�c��H+����
| ||
| B�����Һ�У�c��NH3H2O��+c��NH4+��=0.5a mol?L-1 | ||
| C��a=b | ||
| D�����Һ�У�c��H+��+c��NH4+��=c��OH-��+c��Cl-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com