
【题目】在常温常压下,将三个分别盛满氨气、氯化氢与空气体积比为3∶1的混合气、二氧化氮的等容积烧瓶,再分别倒置于盛水的水槽中,当水进入烧瓶中,并使气体充分溶解后,假定烧瓶中溶液无损失,所得溶液的物质的量浓度之比为
A.1∶1∶1 B.5∶5∶4 C.1∶2∶3 D.1∶1∶2
【答案】A
【解析】本题主要考查物质的量浓度的计算。盛有氨气的烧瓶倒立在水槽中时,水会充满整个烧瓶;氯化氢与空气体积比为3∶1的混合气倒立在水槽中时,盐酸完全溶于水,水会充入烧瓶的![]() ;二氧化氮和水反应:3NO2+2H2O=2HNO3+NO,根据方程式知,水会充入烧瓶的
;二氧化氮和水反应:3NO2+2H2O=2HNO3+NO,根据方程式知,水会充入烧瓶的![]() ,溶液中的溶质是硝酸,其物质的量是二氧化氮的
,溶液中的溶质是硝酸,其物质的量是二氧化氮的![]() ;相同条件下,等体积的气体其物质的量相等,令气体的物质的量为a mol,假设烧瓶的体积是VL,三种溶液中溶质的物质的量分别是:n(NH3)=amol,n(HCl)=amol×
;相同条件下,等体积的气体其物质的量相等,令气体的物质的量为a mol,假设烧瓶的体积是VL,三种溶液中溶质的物质的量分别是:n(NH3)=amol,n(HCl)=amol×![]() ,n(HNO3)=amol×
,n(HNO3)=amol×![]() ,三种溶液的体积分别是V(NH3)= VL,V(HCl)=
,三种溶液的体积分别是V(NH3)= VL,V(HCl)= ![]() VL,V(HNO3)=
VL,V(HNO3)=![]() VL,根据c=
VL,根据c=![]() 可知,c(NH3)=c(HCl)=c(NO2)=
可知,c(NH3)=c(HCl)=c(NO2)=![]() mol/L,所以其浓度之比为1∶1∶1。答案选A。
mol/L,所以其浓度之比为1∶1∶1。答案选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L He ③4℃ 9mL 水 ④0.2mol H3PO4
A. ①④③② B. ④③②①
C. ②③④① D. ①④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是学习和研究化学的一种重要方法。下列分类合理的是( )
A. K2CO3和K2O都属于盐 B. H2SO4和HNO3都属于酸
C. KOH和Na2CO3都属于碱 D. Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和甲烷催化合成CO和H2是CO2资源化利用的有效途径。主要反应为
Ⅰ:CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
(1)已知CH4(g)+H2O(g) ![]() CO(g)+H2(g) △H=+206kJ/mol
CO(g)+H2(g) △H=+206kJ/mol
写出CH4和水蒸气反应生成CO2的热化学方程式_________。
(2)在恒温、恒容的密闭容器中发生反应I,下列选项能够说明反应I达到平衡状态的是______。
A.混合气体的密度不变
B.混合气体的总压强不变
C.CH4、CO2、CO、H2的物质的量之比为1:1:2:2
D.3V正(H2)=V逆(CH4)
E.混合气体的平均相对分子质量不变
(3)催化合成的温度通常维持在550-750℃之间,从反应速率角度分析其主要原因可能是_________。
(4)将CH4与CO2各1mol充入某密闭容器中,发生反应I。100Kpa时,反应I到达平衡时CO2的体积分数与温度的关系曲线如图所示。
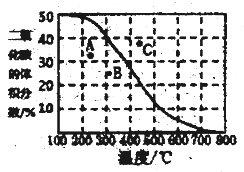
①图中A、B、C三点表示不同温度、压强下达到平衡时CO2的体积分数,则______点对应的平衡常数最小,判断依据是________;__________点对应的压强最大。
②300℃,100Kpa下,该容器中反应I经过40min达到平衡,计算反应在0-40min内的平均反应速率为v(CO2)=_________mol/min(结果保留两位有效数字),该温度下的压强平衡常数Kp=________。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质或原子结构的递变,叙述不正确的是( )
A. Na、Mg、Al原子最外层电子数依次增多 B. P、S、Cl得电子能力依次增强
C. Li、Na、K的电子层数依次增多 D. C、N、O元素最高正化合价依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。X的激发态原子电子排布式为2p1,Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Z的基态原子中有3个未成对电子,W的电离能如下表所示,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
元素 | 第一电离能 | 第二电离能 | 第三电离能 |
W | 495.8 | 4562 | 6910.3 |
(1)U原子电子排布式为_______________。
(2)X与Z 形成的化合物Z2X4,Z原子采取的杂化轨道类型为_______,Y的最高价氧化物的水化物的正盐的阴离子的空间构型为_______;
(3)W的氯化物和Mg的氯化物中,熔点较高的是________(填化学式),原因是_______。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1:3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,写出I4O9的电离方程式______。
(5)Nb(黑球)和I(白球)能形成一种线性的无机高分子化合物,其结构是许多八面体通过棱边而联结起来的长链,如下图所示。则该化合物中Nb和I的原子个数比为______。
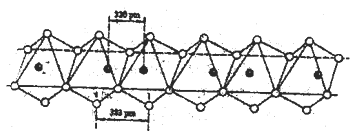
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组固体物质,可按照溶解、过滤、蒸发的实验操作顺序,将它们相互分离的是
A.NaNO3和NaClB.CuO和木炭粉
C.MnO2和KClD.BaSO4和AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:
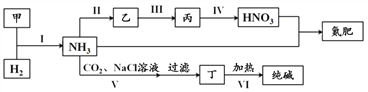
下列说法不正确的是( )
A. 甲、乙、丙三种物质中都含有氮元素
B. 反应II、III和Ⅳ的氧化剂相同
C. VI的产物可在上述流程中被再次利用
D. V中发生反应:NH3 + CO2 + H2O + NaCl === NaHCO3↓+ NH4Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com