
����Ŀ��C��N��S�������ﳣ�����һЩ�������⣬���й����������о��ø��ֻ�ѧ������������Щ���ʶԻ����IJ���Ӱ�졣
(1)��֪��2CO(g)��O2(g)=2CO2(g) ��H1=��566kJ/molS(l)��O2(g)=SO2(g) ��H2=��296kJ/mol
һ�������£�����ͨ��CO��SO2��Ӧ����S(1)��һ���������壬ʵ��ȼú��������Ļ��գ�д���÷�Ӧ���Ȼ�ѧ����ʽ_______________________________��
(2)��500���ºϳɼ״��ķ�Ӧԭ��Ϊ��
CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)����1L���ܱ������У�����1mol CO2��3mol H2��ѹǿΪp0 kpa�����CO2(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��(���淴Ӧ��ƽ�ⳣ��������ƽ��Ũ�ȼ��㣬Ҳ������ƽ���ѹKp����ƽ��Ũ�ȣ������ѹ=��ѹ�����ʵ�������)
CH3OH(g)��H2O(g)����1L���ܱ������У�����1mol CO2��3mol H2��ѹǿΪp0 kpa�����CO2(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��(���淴Ӧ��ƽ�ⳣ��������ƽ��Ũ�ȼ��㣬Ҳ������ƽ���ѹKp����ƽ��Ũ�ȣ������ѹ=��ѹ�����ʵ�������)

��0~4min��H2��ƽ����Ӧ����v(H2)=________mol��L1��min1��
��CO2ƽ��ʱ���������Ϊ______________�����¶���KpΪ_________kPa-2_(�ú���p0��ʽ�ӱ�ʾ��С�������1λ)��
��������˵���÷�Ӧ�Ѵﵽƽ��״̬����______________��
A��v��(CH3OH)=3v��(H2)
B��CO2��H2��CH3OH��H2OŨ��֮��Ϊ1��3��1��1
C�����º�ѹ�£������������ٱ仯
D�����º����£�������ܶȲ��ٱ仯
��500�桢��2���ݻ�����2L���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
���� | ������ | ������ |
��Ӧ����ʼͶ���� | 1mol CO2��3mol H2 | 0.5mol CO2��1mol H2 1mol CH3OH��1mol H2O |
CH3OH��ƽ��Ũ��/mol��L1 | C1 | C2 |
���������з�Ӧ��ʼ��________(��������Ӧ�������淴Ӧ��)������У�c1_________(����>����<������=��)c2��
���𰸡�2CO(g)��SO2(g)=S(l)��2CO2(g) ��H=��270kJ/mol 0.375 10% 256/3p02 C �淴Ӧ <
��������
��1������ԭ���غ㣬CO��SO2��Ӧ����S��1����һ������������CO2����ѧ����ʽΪ2CO��g��+SO2��g��=S��l��+2CO2��g����������������Ȼ�ѧ����ʽ��ϸ�˹���ɽ������㡣
��2���ٽ��![]() ���㣻
���㣻
�ڷ�Ӧ���е�15minʱ�������Ũ�Ȳ��䣬��ʱ�ﵽƽ��״̬����������ʽ�������������
�۴ﵽƽ��ʱ�����淴Ӧ������ȣ��Ҹ����ʵ�Ũ�Ȳ��䣬�Դ��ж��Ƿ�ƽ��״̬��
�ܿɸ�������ͼ�����Ӧ��ƽ�ⳣ������������Ͷ�Ϲ鵽�ұ��൱����1mol�״���1molˮ������
����1������ԭ���غ㣬���ɵ��������Ƕ�����̼�������ķ�ӦΪ2CO��g��+SO2��g��=S��l��+2CO2��g��������������Ȼ�ѧ����ʽ�����������α��Ϊ�ٺ͢ڣ����ݸ�˹���ɢ�-�ڿɵ�����Ӧ���Ȼ�ѧ����ʽ����2CO��g��+SO2��g��=S��l��+2CO2��g����H=-566kJ/mol-��-296kJ/mol��=-270kJ/mol��
�ʴ�Ϊ��2CO��g��+SO2��g��=S��l��+2CO2��g����H=-270kJ/mol��
��2����0��4 min��CO��Ũ�ȼ�����0.5mol/L����������Ũ�ȼ�����1.5mol/L��H2��ƽ����Ӧ����v��H2��=1.5mol/L��4min=0.375molL-1min-1��
�ʴ�Ϊ��0.375��
�ڷ�Ӧ

CO2ƽ��ʱ�������������Ũ�Ȱٷֱȣ���![]() ����ʼʱ����1 mol CO2��3 mol H2��ѹǿΪp0 ��ƽ��ʱ�����������ʵ���Ϊ2.5mol��ѹǿΪ0.625p0 ��
����ʼʱ����1 mol CO2��3 mol H2��ѹǿΪp0 ��ƽ��ʱ�����������ʵ���Ϊ2.5mol��ѹǿΪ0.625p0 ��
 ��
��
�ʴ�Ϊ��10%��256/3p02��
��A��v����CH3OH��=3v����H2��˵�����淴Ӧ���ʲ���ȣ��ʲ���˵����Ӧ�Ѵ�ƽ�⣬��A����
B��CO2��H2��CH3OH��H2OŨ��֮��Ϊ1��3��1��1����Ͷ���йأ�����˵����Ӧ�Ѵ�ƽ�⣬��B����
C�����º�ѹ�£������������ٱ仯��˵����Ӧ�Ѵ�ƽ�⣬��C��ȷ��
D�����º����£�������ܶȲ���һ�����������䲻�ٱ仯������˵����Ӧ�ﵽƽ�⣬��D����
�ʴ�Ϊ��C��
��������Qc=![]() =8���ɸ�������ͼ�����Ӧ��ƽ�ⳣ��
=8���ɸ�������ͼ�����Ӧ��ƽ�ⳣ��![]() =5.3��Qc��K��ƽ��������С���������Ͷ�Ϲ鵽�ұ��൱����1mol�״���1molˮ��������������ƽ��ʱc1��c2��
=5.3��Qc��K��ƽ��������С���������Ͷ�Ϲ鵽�ұ��൱����1mol�״���1molˮ��������������ƽ��ʱc1��c2��
�ʴ�Ϊ���淴Ӧ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H��һ���ʼIJ����м��塣ʵ�����ɷ�����A�Ʊ�H��һ�ֺϳ�·�����£�
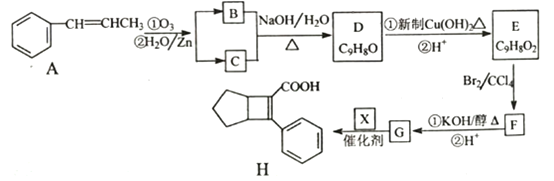
��֪����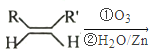 RCHO+RCHO
RCHO+RCHO
��RCHO+RCH2CHO![]() +H2O
+H2O
��![]()
��ش��������⣺
��1�����㻯����B������Ϊ_________��C��ͬϵ������Է���������С�Ľṹ��ʽΪ__________��
��2����E����F�ķ�Ӧ����Ϊ_________��
��3��X�Ľṹ��ʽΪ_________��
��4��д��D����E�ĵ�������Ӧ�Ļ�ѧ����ʽ_______________��
��5��G���Ҵ�����������Ӧ���ɻ�����Y��Y�ж���ͬ���칹�壬���з�������������ͬ���칹����____�֣�д����������һ�ֵĽṹ��ʽ________��
�������к��б����������뱥��̼��������Һ��Ӧ�ų�CO2��
����˴Ź���������ʾ��4�ֲ�ͬ��ѧ���������⣬�ҷ����֮��Ϊ6��2��1��1��
��6��д����![]() Ϊԭ���Ʊ�������
Ϊԭ���Ʊ�������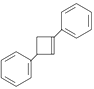 �ĺϳ�·�ߣ��������Լ���ѡ��________
�ĺϳ�·�ߣ��������Լ���ѡ��________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ྦྷ�������������صĹؼ����ϡ��������ɴֹ��Ʊ��ྦྷ��ļ����̡�
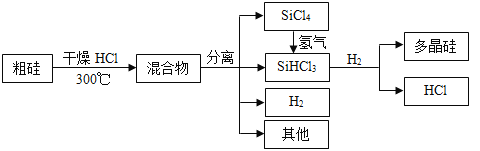
�ش��������⣺
���������![]() ��300��ʱ��Ӧ����
��300��ʱ��Ӧ����![]() �����
�����![]() ���ų�
���ų�![]() �������÷�Ӧ���Ȼ�ѧ����ʽΪ________________________��
�������÷�Ӧ���Ȼ�ѧ����ʽΪ________________________��![]() �ĵ���ʽΪ__________________��
�ĵ���ʽΪ__________________��
������![]() �⻯Ϊ
�⻯Ϊ![]() �����ַ�������Ӧ�ķ�Ӧ����Ϊ��
�����ַ�������Ӧ�ķ�Ӧ����Ϊ��
��![]()
![]()
��![]()
![]()
��![]()
![]()
��1���⻯����������ĸߴ���![]() ���ö��Ե缫���
���ö��Ե缫���![]() ��Һ�Ʊ���д������
��Һ�Ʊ���д������![]() �ĵ缫����______���������������������������õ缫��Ӧ����ʽΪ________________________��
�ĵ缫����______���������������������������õ缫��Ӧ����ʽΪ________________________��
��2����֪��ϵ�����ܱ�![]() ��
��![]() ʱ��Ӧ�Է����С������⻯��Ӧ��
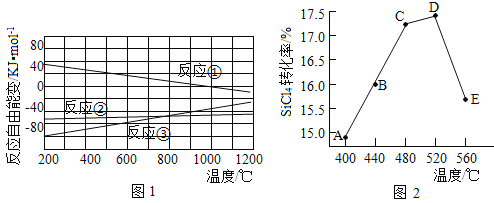
ʱ��Ӧ�Է����С������⻯��Ӧ��![]() ���¶ȵĹ�ϵ��ͼ1��ʾ����֪����Ӧ�����Է����е�����¶���____________����ͬ�¶��£���Ӧ���ȷ�Ӧ����
���¶ȵĹ�ϵ��ͼ1��ʾ����֪����Ӧ�����Է����е�����¶���____________����ͬ�¶��£���Ӧ���ȷ�Ӧ����![]() С����Ҫԭ����________________________��
С����Ҫԭ����________________________��
��3����ͬ�¶��·�Ӧ����![]() ת������ͼ2��ʾ������������ȷ����______������ţ���
ת������ͼ2��ʾ������������ȷ����______������ţ���
a��B�㣺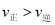 b��
b��![]() ��A��
��A��![]() �� c����Ӧ�����¶ȣ�
�� c����Ӧ�����¶ȣ�![]() ��
��
��4����Ӧ����![]() ______����
______����![]() ��
��![]() ��ʾ�����¶����ߣ���Ӧ����ƽ�ⳣ��
��ʾ�����¶����ߣ���Ӧ����ƽ�ⳣ��![]() ______������������������С����������������
______����������������������������������
��5���ɴֹ��Ʊ��ྦྷ�������ѭ��ʹ�õ����ʳ�![]() ��
��![]() ��
��![]() �⣬����______�������ʽ����
�⣬����______�������ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮú���任[CO(g)+H2O(g)=CO2(g)+H2(g)]����Ҫ�Ļ������̣���Ҫ���ںϳɰ��������Լ��ϳ����ӹ��ȹ�ҵ�����С��ش��������⣺
(1)Shibata����������ʵ�飺��ʹ��H2������ͨ������721 ���µĹ���������CoO(s)�������ܲ��ֱ���ԭΪ������(Co)��ƽ���������H2�����ʵ�������Ϊ0.0250��
����ͬһ�¶�����CO��ԭCoO(s)��ƽ���������CO�����ʵ�������Ϊ0.0192����������ʵ�����жϣ���ԭCoO(s)ΪCo(s)��������CO_________H2(��������������С����)��
(2)721 ��ʱ�����ܱ������н������ʵ�����CO(g)��H2O(g)��ϣ������ʵ��Ĵ������з�Ӧ����ƽ��ʱ��ϵ��H2�����ʵ�������Ϊ_________(����)��
A����0.25 B��0.25 C��0.25��0.50 D��0.50 E����0.50
(3)�ҹ�ѧ�߽��ʵ��������ģ�������о����ڽ����������ˮú���任�ķ�Ӧ���̣���ͼ��ʾ�����������ڽ���������ϵ�������![]() ��ע��
��ע��
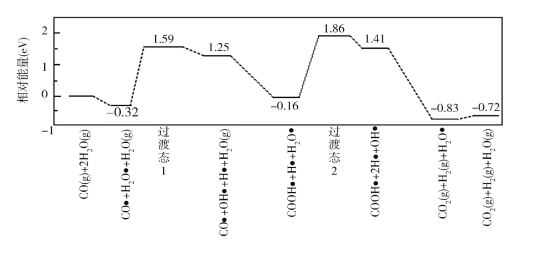
��֪ˮú���任����H________0(����������������������С����)�����������������(���)E��=_________eV��д���ò���Ļ�ѧ����ʽ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A. ����������Һ�м�������泥�Ba2����OH����NH4+��SO42-=BaSO4����NH3��H2O
B. �ö��Ե缫���CuCl2��Һ��Cu2����2Cl����2H2O![]() Cu(OH)2����H2����Cl2��
Cu(OH)2����H2����Cl2��
C. ��Ư����Һ��ͨ��������������Ca2����2ClO����SO2��H2O=CaSO3����2HClO
D. ������Һ��ͨ��������CO2��C6H5O����CO2��H2O��C6H5OH��HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��IJ��C6H12O6�����������������Ʊ����ᣬװ����ͼ1��ʾ�����ȡ�����������̶�װ�þ�����ȥ����ʵ��������£�
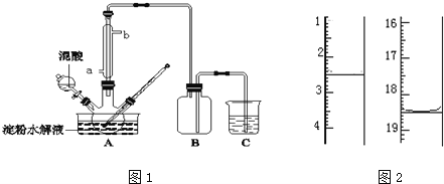
�ٽ�1��1�ĵ���ˮ��Һ���������ᣨ98%�������ձ��У�ˮԡ������85�桫90��������30min��Ȼ�����¶Ƚ���60�����ң�
�ڽ�һ�����ĵ���ˮ��Һ����������ƿ�У�
�ۿ��Ʒ�ӦҺ�¶���55��60�������£��߽�������μ�һ�����������������Ļ��ᣨ65%HNO3��98%H2SO4��������Ϊ2��1.5����Һ��
�ܷ�Ӧ3h���ң���ȴ����ѹ���˺����ؽᾧ�ò��ᾧ�壬������������ˮ��Һ�����пɷ������з�Ӧ��
C6H12O6+12HNO3��3H2C2O4+9NO2��+3NO��+9H2O
C6H12O6+8HNO3��6CO2+8NO��+10H2O
3H2C2O4+2HNO3��6CO2+2NO��+4H2O
��ش��������⣺
��1��ʵ��ټ���98%���������������ǣ�_________��
��2��ʵ����������μӹ��죬�����²�������½�����ԭ����_________��
��3����������Ƿ�ˮ����ȫ���õ��Լ�Ϊ_________��
��4�������ؽᾧ�ļ�ѹ���˲����У����ձ����������⣬������ʹ�����ڹ����β��ϵ�������_________��
��5������Ʒ�ں�������Լ90�����º�������أ��õ���ˮ�ϲ��ᣮ��KMnO4����Һ�ζ����÷�Ӧ�����ӷ���ʽΪ��2MnO4��+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��ȡ����Ʒ0.12g��������ˮ��ȫ�ܽ⣬Ȼ����0.020molL��1������KMnO4��Һ�ζ����յ㣨���ʲ����뷴Ӧ������ʱ��Һ��ɫ�仯Ϊ_________���ζ�ǰ��ζ����е�Һ�������ͼ2��ʾ����ò��ᾧ����Ʒ�ж�ˮ�ϲ������������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������ݣ�7.2��10-4��4.6��10-4��4.9��10-10�ֱ��������йص�������ĵ��볣��������֪���з�Ӧ���Է�����
NaCN+HNO2![]() HCN+NaNO2 NaCN+HF
HCN+NaNO2 NaCN+HF![]() HCN+NaF NaNO2+HF
HCN+NaF NaNO2+HF![]() HNO2+NaF
HNO2+NaF
�ɴ˿��ж�������������ȷ����
A.K��HF��=7.2��10-4B.K��HNO2��=4.9��10-10
C.����������Ӧ���ɵó�����D.K��HCN��<K(HNO2)<K(HF)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������0.1000mol/L������ֱ���μ��뵽20.00mL0.1000 mo1/L������һԪ��MOH��XOH��YOH��Һ��,��Һ��pH�������������ı仯��ͼ��ʾ�� ����˵������ȷ����

A. XOHΪǿ��,MOH��YOH�� Ϊ����
B. V(HCl)=15.00mLʱ,������Һ��������Ũ�ȴ�С˳��: XOH>MOH>YOH
C. ������μ���20.00 mLʱ,�������߸պ��ཻ
D. ����μ���������40.00mL�Ĺ�����,������Һ��ˮ�ĵ���̶Ⱦ���������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ�����ϩ������ķ�Ӧװ����ͼ��ʾ���й���Ϣ���£�
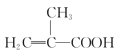 +CH3OH
+CH3OH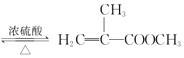 +H2O
+H2O

��֪����ϩ����������ۺϣ�����ϩ�����������Һ���ܽ�Ƚ�С��CaCl2���봼����γɸ����
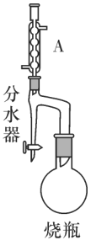
ʵ�鲽�裺
����100mL��ƿ�����μ��룺15mL����ϩ�ᡢ2����ʯ��10mL��ˮ�״���������Ũ���
���ڷ�ˮ����Ԥ�ȼ���ˮ��ʹˮ���Ե��ڷ�ˮ����֧�ܿڣ�ͨ������ˮ������������ƿ���ڷ�Ӧ�����У�ͨ����ˮ���²��������ֳ����ɵ�ˮ�����ַ�ˮ����ˮ��Һ��ĸ߶Ȳ��䣬ʹ�Ͳ㾡���ص�Բ����ƿ�У�
�۵�____��ֹͣ���ȣ�
����ȴ�����Լ�Xϴ����ƿ�еĻ����Һ�����룻
��ȡ�л�����Һ���õ��ϴ����ļ���ϩ�������
��ش��������⣺
��1��Aװ�õ�������__��
��2���뽫�����������__��
��3������ʵ��������ɵĸ�����ṹ��ʽΪ__(������)��
��4������˵����ȷ����___(����ĸ����)��
A.�ڸ�ʵ���У�Ũ�����Ǵ�������ˮ��
B.������Ӧ�������ɵ������ܶȱ�ˮ�����÷�ˮ����߷�Ӧ���ת����
C.ϴ�Ӽ�X��һ���Լ�������Ҫ�����ñ���Na2CO3������CaCl2��Һϴ��
D.Ϊ����������ٶȣ����һ������ɲ��ü�ѹ���ò���һ�������ó�ѹ����
��5��ʵ������ռ���ˮ���������ˮ�����������Ϊ2.70g���������ϩ������IJ���ԼΪ__(�������һλС��)��ʵ���м���ϩ�������ʵ�ʲ�������С�ڴ˼���ֵ��������ԭ����__(����ĸ����)��
A.��ˮ���ռ���ˮ�ﺬ����ϩ�����
B.ʵ�������·�������Ӧ
C.��Ʒ����ʱ�ռ����ֵͷе�����
D.��Ʒ��ϴ�ӡ���������������ʧ.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com