
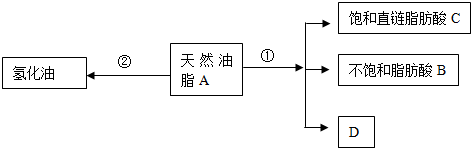
分析 (1)假设B的分子式为C9nH16nOn,根据B的相对分子质量为280,原子个数比为C:H:O=9:16:1解题;
(2)分子中原子或基团被其他原子或原子团所取代的反应称取代反应;A的水解可以表示成:C57H106O6+3H2O→C3H8O3(甘油)+C18H32O2+2C;
(3)地沟油的主要成分为油脂,属于酯类,故可以在碱性条件下水解制取肥皂,由于含有重金属离子和细菌,故不能食用,据此分析;
(4)油脂是高级脂肪酸甘油酯,水解生成甘油,甘油含有羟基,羟基能与钠反应.
解答 解:(1)假设B的分子式为C9nH16nOn,有12×9n+1×16n+16×n=280,求得n=2,所以B的分子式为C18H32O2,故答案为:C18H32O2;
(2)油脂的水解是取代反应,A的水解可以表示成:C57H106O6+3H2O→C3H8O3(甘油)+C18H32O2+2C,根据原子守恒可知C的分子式为:C18H36O2,结合C是直链饱和脂肪酸,可知C的结构简式为:CH3-(CH2)16-COOH,是硬脂酸,C原子和H原子个数分别为18和36,故答案为:取代反应;18;36;
(3)A.地沟油的主要成分为油脂,属于酯类,故可以在碱性条件下水解制取肥皂,故A正确;
B.地沟油的主要成分是油脂,属于酯类,故B正确;
C.地沟油可以水解属于酯类,子酸性或碱性条件下可以水解,故C正确;
D.地沟油含有重金属离子和细菌,不能适用,故D错误.
故选D.
(4)油脂是高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油,甘油含有羟基,羟基能与钠反应:2C3H5(OH)3+6Na→2C3H5(ONa)3+3H2↑,
故答案为:2C3H5(OH)3+6Na→2C3H5(ONa)3+3H2↑.
点评 本题考查有机物的推断、取代和加成反应、水解反应等,难度不大,注意油脂的氢化属于加成反应,油脂的皂化属于取代反应.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | O=O | H-O |
| 键能(KJ/mol) | 436 | 496 | 463 |
| A. | 242 | B. | -242 | C. | 484 | D. | -484 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
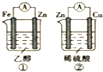
| A. | ①、②装置都能将化学能转化为电能 | |
| B. | ②中的硫酸根离子向负极移动 | |
| C. | ②中的电子轴Zn经过导线流向Cu | |
| D. | ②中铜片上发生的电极反应式为2H++2e-=2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.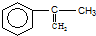 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下: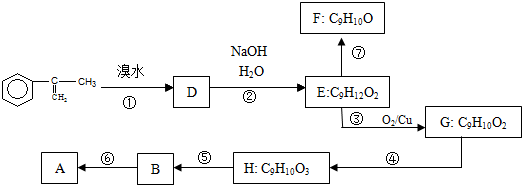
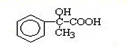
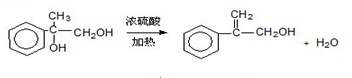 .两分子H之间发生反应生成六元环酯化学方程式是:2
.两分子H之间发生反应生成六元环酯化学方程式是:2 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$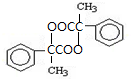 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H5OH | C. | C3H8O | D. | C3H8O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
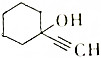 将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮(
将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮( 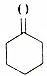 ),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )
),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )| A. | 1:1 | B. | 1:2 | C. | 13:49 | D. | 24:49 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
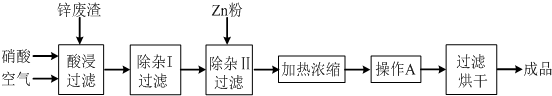
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②③ | C. | ①④ | D. | ①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com