
分析 根据各物质的转化关系,A[CH2=C(CH3)2]与溴化氢发生加成反应生成卤代烃,再碱性水解得醇,根据D的分子式可知,C再氧化得D为羧酸,D发生题中信息中的取代反应生成E,所以可推得B为CH2BrCH(CH3)2,C为HOCH2CH(CH3)2,D为HOOCCH(CH3)2,E为HOOCCBr(CH3)2,据此答题.
解答 解:根据各物质的转化关系,A[CH2=C(CH3)2]与溴化氢发生加成反应生成卤代烃,再碱性水解得醇,根据D的分子式可知,C再氧化得D为羧酸,D发生题中信息中的取代反应生成E,所以可推得B为CH2BrCH(CH3)2,C为HOCH2CH(CH3)2,D为HOOCCH(CH3)2,E为HOOCCBr(CH3)2,
(1)根据A的结构简式可知,A的系统命名为2-甲基丙烯,B→C的反应类型是取代(水解)反应,
故答案为:2-甲基丙烯;取代(水解)反应;
(2)C为HOCH2CH(CH3)2,C的一种同类别的同分异构体M,M能发生催化氧化反应生成醛,说明与羟基相连的碳上有两个氢原子,则M的结构简式为,
故答案为:CH3CH2CH2CH2OH;
(3)E为HOOCCBr(CH3)2,E与足量的氢氧化钠溶液供热反应的化学方程式为HOOCCBr(CH3)2+2NaOH→NaOOCCOH(CH3)2+NaBr+H2O,
故答案为:HOOCCBr(CH3)2+2NaOH→NaOOCCOH(CH3)2+NaBr+H2O.
点评 本题考查有机物的推断,难度中等,需要学生对给予的信息进行利用,较好的考查学生自学能力与知识迁移运用.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
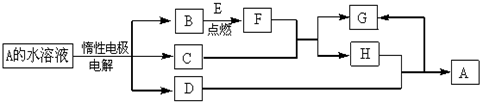
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的分子式:CH2=CH2 | |
| B. | NaHCO3的电离:HCO3-+H2O?H3O++CO32- | |
| C. | NaOH的结构式:Na-O-H | |
| D. | NH4Cl的电子式: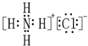 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,E原子的价电子排布式为3s23p5,F在周期表中的位置是第四周期第IVB族.
,E原子的价电子排布式为3s23p5,F在周期表中的位置是第四周期第IVB族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴入石蕊呈红色,滴入甲基橙则呈黄色,则该溶液的pH值可能为4.4~5.0 | |
| B. | 电解水时加入H2SO4、NaOH、CuCl2等电解质均可增加导电性,而会使电解水的速率增大 | |
| C. | 配制标准NaOH溶液的NaOH固体含有少量的KOH,此时中和测得盐酸的浓度数值一定偏高 | |
| D. | 电解饱和食盐水一段时间,若向某一极滴入酚酞试液后溶液呈红色,该极一定是阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
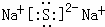 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 1mol•L-1FeCl3溶液中含阳离子数为0.1NA | |
| B. | 标准状况下,2.24L乙醛完全燃烧所得CO2分子数为0.2NA | |
| C. | 0.6gCaCO3与KHCO3的混合物中所含质子数为0.3NA | |
| D. | 80Ml 10mol•L-1浓盐酸与足量MnO2反应,转移电子数为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com