
【题目】A~G是几种烃分子的球棍模型,据此回答下列问题:

(1)书写结构简式:C____________F_____________
(2)能够发生加成反应的烃有________(填数字)种。
(3)一卤代物种类最多的是________(填对应字母)。
(4)等质量的上述六种烃,完全燃烧时消耗O2最多的是________(填对应字母)。等物质的量的上述六种烃,完全燃烧时消耗O2最多的是________(填对应字母)。
(5)在120 ℃,1.01×105 Pa下与足量O2混合点燃,完全燃烧后气体体积没有变化的烃是________(填对应字母)。
(6)常温下含碳量最高的烃是________(填对应字母)。
(7)写出F发生溴代反应的化学方程式_________________________________。
【答案】 CH2=CH2 ![]() 4 G A G AC F
4 G A G AC F ![]()
【解析】根据结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,则
(1)C和F的结构简式分别是CH2=CH2、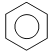 ;(2)能够发生加成的烃有有乙烯、乙炔、苯和甲苯4种;(3)一卤代物种类最多的是甲苯,共有4种,故答案为:G;(4)烃分子含氢量越高,消耗氧气越多。则等质量的上述六种烃,完全燃烧时消耗O2最多的是甲烷,答案选A;如果烃分子的分子式为CxHy,则烃分子中(x+y/4)越大,等物质的量时消耗氧气越多,因此完全燃烧时消耗O2最多的是甲苯,答案选G。(5)烃燃烧120℃时水为气体,依据燃烧通式分析,CxHy+(x+y/4)O2→xCO2+y/2H2O(g),反应前后压强不变即气体物质的量不变,1+x+y/4=x+y/2,解得y=4;所以烃分子式中氢原子为4的符合,故甲烷和乙烯符合,故答案为:AC;(6)根据分子式可计算常温下含碳量最高的烃是苯,答案选F。(7)F发生溴代反应的化学方程式为
;(2)能够发生加成的烃有有乙烯、乙炔、苯和甲苯4种;(3)一卤代物种类最多的是甲苯,共有4种,故答案为:G;(4)烃分子含氢量越高,消耗氧气越多。则等质量的上述六种烃,完全燃烧时消耗O2最多的是甲烷,答案选A;如果烃分子的分子式为CxHy,则烃分子中(x+y/4)越大,等物质的量时消耗氧气越多,因此完全燃烧时消耗O2最多的是甲苯,答案选G。(5)烃燃烧120℃时水为气体,依据燃烧通式分析,CxHy+(x+y/4)O2→xCO2+y/2H2O(g),反应前后压强不变即气体物质的量不变,1+x+y/4=x+y/2,解得y=4;所以烃分子式中氢原子为4的符合,故甲烷和乙烯符合,故答案为:AC;(6)根据分子式可计算常温下含碳量最高的烃是苯,答案选F。(7)F发生溴代反应的化学方程式为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】环境污染已严重危害人类的生活。下列对应关系正确的是
选项 | 环境问题 | 造成环境问题的主要物质 |
A | 酸雨 | O3 |
B | 温室效应 | CO2 |
C | 南极臭氧层空洞 | SO3 |
D | 光化学烟雾 | N2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生活、社会可持续发展密切相关,下列说法正确的是
A.地球上最基本的能源是化学能
B.太阳能热水器、沼气的使用、玉米制乙醇都涉及生物质能的利用
C.利用二氧化碳制造全降解塑料能有效减少“白色污染”
D.人们可以把放热反应释放的能量转化为其它可利用的能量,而吸热反应没有利用价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2===2H2O,下列有关说法正确的是( )

A.电子通过外电路从b极流向a极
B.b极上的电极反应式为O2+2H2O+4e-===4OH-
C.每转移0.1 mol电子,便消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A.氧化物:CO2、NO、SO2、H2O
B.碱:NaOH、KOH、Ba(OH)2、Na2CO3
C.铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3H2O
D.碱性氧化物:Na2O、CaO、Mn2O7、Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用于净化汽车尾气的反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为l×1059。下列说法正确的是( )
2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为l×1059。下列说法正确的是( )
A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
B.提高尾气净化效率的常用方法是升高温度
C.提高尾气净化效率的最佳途径是研制高效催化剂
D.570K时该反应正向进行的程度很大,故使用催化剂并无实际意义
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2015福建]下列制作铅笔的材料与相应工业不对应的是
A.橡皮擦——橡胶工业
B.铝合金片——冶金工业
C.铅笔芯——电镀工业
D.铅笔漆——涂料工业
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25℃时,取10mL 0.1mol/L醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1000mL,溶液pH数值范围为___________,溶液中![]() ___________(填“增大”“减小”“不变”或“不能确定”)。
___________(填“增大”“减小”“不变”或“不能确定”)。
②25℃时,0.1mol/L氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________,25℃时,氨水电离平衡常数约为___________。
(2)25℃时,现向10mL0.1mol/L氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中![]() ___________(填序号)。
___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL0.1mol/LNaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母)。
图中M、Q、N三点所示溶液中水的电离程度最大的点是___________(填字母)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com