

| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
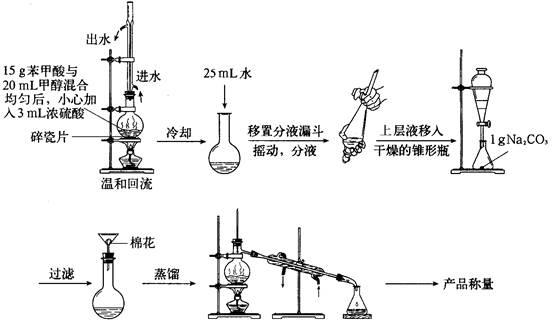

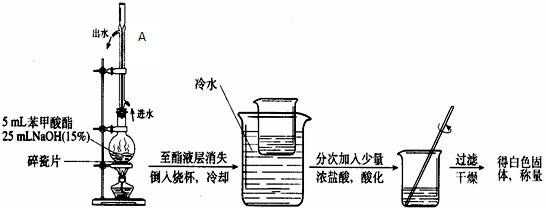
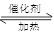 C6H5COOCH3+H218O 。(2分)
C6H5COOCH3+H218O 。(2分)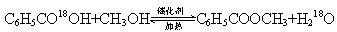


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作、现象 | 解释、结论 |
| A. | 铜片放入浓硫酸中,无明显变化 | 铜在冷的浓硫酸中会发生钝化 |
| B. | 往某氯化物溶液中滴加氨水,产生白色沉淀 | 该氯化物是AlCl3 |
| C. | 将10ml某pH=3的HA溶液加水稀释到100ml,所得溶液pH=3.8 | HA是弱酸 |
| D. | 往MgCl2溶液中滴加NaOH溶液,调至pH=9时,开始出现沉淀[已知Mg(OH)2的Ksp=5.6×10-12] | 原溶液中 c(Mg2+)=5.6×10-2mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
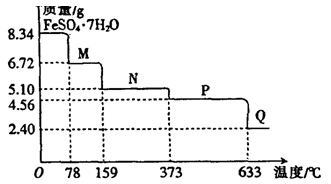
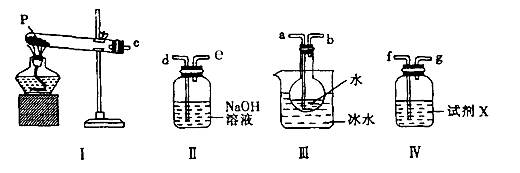
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.KI溶液 | B.淀粉溶液 | C.NaOH溶液 | D.稀H2SO4E.氯水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 |
| B.用萃取的方法分离汽油和煤油 |
| C.用溶解、过滤的方法分离KNO3和NaCl固体的混合物 |
| D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
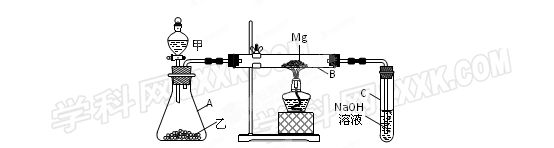 (1)选择制取SO2的最合适试剂 (填序号)。
(1)选择制取SO2的最合适试剂 (填序号)。
 ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
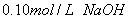 溶液,将其中一份放在空气中一段时间后,溶液的pH (填“增大”“减小”或“不变”)其原因是 。用已知浓度的盐酸中和上述两份溶液。若中和放在空气中一段时间后的那份溶液消耗盐酸的体积为
溶液,将其中一份放在空气中一段时间后,溶液的pH (填“增大”“减小”或“不变”)其原因是 。用已知浓度的盐酸中和上述两份溶液。若中和放在空气中一段时间后的那份溶液消耗盐酸的体积为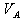 ,中和另一份溶液消耗盐酸的体积为
,中和另一份溶液消耗盐酸的体积为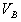 ,则(1)以甲基橙为指示剂
,则(1)以甲基橙为指示剂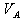 和
和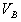 的关系是 。(2)以酚酞为指示剂时,
的关系是 。(2)以酚酞为指示剂时,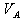 和
和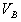 的关系是 。
的关系是 。| A.在250mL的容量瓶中定容配成250mL烧碱溶液 |
| B.用移液管移取25mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙 |
| C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解 |
| D.将物质的量浓度为C的标准硫酸溶液装入酸式滴定管,调节液面,记下开始读数为V1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.仅用硝酸银溶液便可鉴别亚硝酸钠和食盐 |
| B.减压过滤是为了加快过滤速度,得到较大颗粒的晶体 |
| C.硫酸亚铁铵晶体过滤后用无水乙醇洗涤 |
| D.纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com