
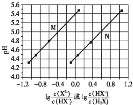
【题目】常温下将NaOH溶液滴加到己二酸![]() 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是![]()
![]()
A.![]() 的数量级为
的数量级为![]()
B.曲线N表示pH与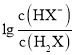 的变化关系
的变化关系
C.NaHX溶液中![]()
D.当混合溶液呈中性时,![]()
【答案】C
【解析】
H2X为二元弱酸,以第一步电离为主,则Ka1(H2X)>Ka2(H2X),酸性条件下,则pH相同时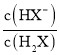 >
>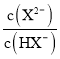 ,由图象可知N为
,由图象可知N为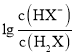 与pH的变化曲线,M为
与pH的变化曲线,M为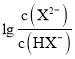 与pH的变化曲线,当
与pH的变化曲线,当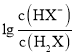 或
或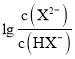 =0时,说明
=0时,说明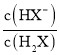 或
或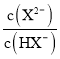 =1,浓度相等,结合图象可计算电离常数并判断溶液的酸碱性。
=1,浓度相等,结合图象可计算电离常数并判断溶液的酸碱性。
A.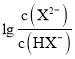 =0时,
=0时,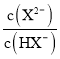 =1,pH=5.4,c(H+)=10-5.4mol/L,则Ka2(H2X)=
=1,pH=5.4,c(H+)=10-5.4mol/L,则Ka2(H2X)=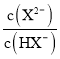 ×c(H+)=c(H+)=10-5.4,可知Ka2(H2X)的数量级为10-6,故A正确;
×c(H+)=c(H+)=10-5.4,可知Ka2(H2X)的数量级为10-6,故A正确;
B.由以上分析可知,曲线N表示pH与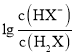 的变化关系,故B正确;
的变化关系,故B正确;
C.由图象可知,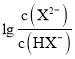 =0时,即c(HX-)=c(X2-),此时pH≈5.4,可知NaHX溶液中HX-电离程度大于HX-水解程度,溶液显酸性,则NaHX溶液呈酸性,溶液中c(H+)>c(OH-),故C错误;
=0时,即c(HX-)=c(X2-),此时pH≈5.4,可知NaHX溶液中HX-电离程度大于HX-水解程度,溶液显酸性,则NaHX溶液呈酸性,溶液中c(H+)>c(OH-),故C错误;
D.由图象可知,当pH=7时,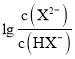 >0,则c(X2-)>c(HX-),所以溶液中存在:c(Na+)>c(X2-)>c(HX-)>c(OH-)=c(H+),故D正确;
>0,则c(X2-)>c(HX-),所以溶液中存在:c(Na+)>c(X2-)>c(HX-)>c(OH-)=c(H+),故D正确;
故答案为C。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】在室温下,下列说法正确的是![]()
![]()
A.在滴有酚酞溶液的氨水里,加入![]() 至溶液恰好无色,则此时溶液的
至溶液恰好无色,则此时溶液的![]()
B.同![]() 的溶液:
的溶液:![]() 溶液,物质的量浓度最大的是
溶液,物质的量浓度最大的是![]()
C.有两种酸HA和HB,已知HA的酸性比HB弱,在物质的量浓度均为![]() 的NaA和NaB混合溶液中,有
的NaA和NaB混合溶液中,有![]()
D.pH相同的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、NaOH溶液,其浓度大小关系为:
溶液、NaOH溶液,其浓度大小关系为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是

A. 3种HCl溶液的c(HCl):最大的是最小的100倍
B. 曲线a、b、c对应的c(NaOH):a>b>c
C. 当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D. 当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)![]() 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.02 mol/(L·s) B.v(B)=0.03 mol/(L·s)
C.v(B)=0.90 mol/(L·min) D.v(C)=0.60 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水钴矿中除SiO2外,还有9.24%CoO、2.78%Fe2O3、0.96%MgO、0.084%CaO。从中提取钴的主要工艺流程如下:

(1)浸出过程中,CoO溶解的离子反应方程式为___,矿渣的主要成分是___、___。
(2)请配平下列除铁的化学方程式:
_Fe2(SO4)3+_H2O+_Na2CO3=_Na2Fe6(SO4)4(OH)12↓+_Na2SO4+_CO2↑
(3)除钙、镁过程中,逐渐加入NaF溶液,当CaF2开始沉淀时,溶液中![]() =___。[已知Ksp(CaF2)=1.0×10-10、Ksp(MgF2)=7.4×10-11]。
=___。[已知Ksp(CaF2)=1.0×10-10、Ksp(MgF2)=7.4×10-11]。
(4)“操作X”是___。进行该操作的主要目的是除去沉淀中的杂质离子,检验杂质中的主要阴离子是否除净的试剂是___。
(5)100t水钴矿最多可获得___tCoC2O44H2O产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色、易潮解,100℃左右时升华。下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不相同,分别如(I)和(Ⅱ)所示,
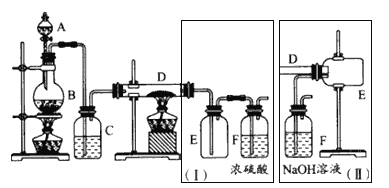
试回答:
(1)B中反应的化学方程式为___________________________。
(2)D中的反应开始前,需排除装置中的空气,应采取的方法是______________。
(3)D中反应的化学方程式为______________________________。
(4)装置(I)的主要缺点是_______________________。
(5)装置(Ⅱ)的主要缺点是______________________________,如果选用此装置来完成实验,则必须采取的改进措施是:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学生用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热。下列说法正确的是( )

A.如图条件下实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是固定小烧杯
D.若改用60mL0.50mol/L盐酸与50mL0.55mol/L的NaOH溶液进行反应,从理论上说所测反应热数值是相等的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究性学习小组利用H2C2O4溶液与酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。实验如表所示,下列有关说法中正确的是( )
实验 序号 | 实验温度/K | 酸性KMnO4溶液 | H2C2O4溶液 | H2O | 溶液褪至无色时所用时间/s | ||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 5 | 0.1 | 3 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 5 | t1 |
A.配制KMnO4溶液时可用稀盐酸酸化
B.若t1<8,则可通过控制变量法由实验A、B探究H2C2O4浓度对化学反应速率的影响并得出结论:增大反应物浓度,化学反应速率加快
C.若span>T1=293K,V1 =V2=3mL,则可通过实验B、C探究温度对化学反应速率的影响
D.利用实验B中数据计算,用KMnO4的浓度变化表示的化学反应速率v(KMnO4)=5×10-4mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com