
��1����50mL 0.50mol��L-1������50mL 0.55mol��L-1NaOH��Һ������ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȡ��ش��������⣺
 ���ձ�����������ĭ���ϵ������� ��
���ձ�����������ĭ���ϵ������� ��
�������ձ��ϸ�Ϊ�DZ����壬��õķ�Ӧ����ֵ��
���ƫ����ƫС������Ӱ�족��
����ͨ���ⶨ�������������Ϊ1.42kJ����д�÷�Ӧ��
�Ȼ�ѧ����ʽ�� ��
��2������֪��CH4(g)��H2O(g)===CO(g)��3H2(g) ��H��+206.2 kJ��mol��1
CH4(g)��CO2(g)===2CO(g)��2H2(g) ��H��+247.4 kJ��mol��1
���Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����CH4(g)��H2O(g)��Ӧ����CO2(g)��H2(g)���Ȼ�ѧ����ʽΪ�� ��
������̬��̬ԭ���γ�1 mol��ѧ���ͷŵ���������м��ܡ���֪�������м�������, ��
N2(g)��3H2(g)  2NH3(g) ��H�� kJ��mol��1��
2NH3(g) ��H�� kJ��mol��1��
| ��ѧ�� | H��H | N��H | N��N |
| ����kJ��mol��1 | 436 | 391 | 945 |
��һ�������£���ˮ��Һ��Ϊ1 mol�������� Cl����ClO����ClO2����ClO3����ClO4��������(kJ)��Դ�С����ͼ��ʾ����3ClO��(aq)===ClO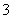 (aq)��2Cl��(aq)�Ħ�H�� kJ��mol��1��
(aq)��2Cl��(aq)�Ħ�H�� kJ��mol��1��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ��Ӧ�У����������ֻ����� Ӧ���͵��ǣ� ����
Ӧ���͵��ǣ� ����
A��2FeCl3��Cu��2FeCl2��CuCl2 �� B��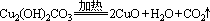
C��4Fe(OH)2+O2+2H2O= 4Fe(OH)3�� D��CaCO3��2HCl��CaCl2��H2O��CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A��Fe3O4��������ϡHNO3��Fe3O4��8H��=Fe2����2Fe3����4H2O
B�������ʵ�����MgCl2��Ba(OH)2 �� HC1 ��Һ��ϣ�Mg2����2OH��= Mg(OH)2��
C����������SO2ͨ��Ca(ClO)2��Һ�У� SO2+ClO��+H2O =HClO+ HSO3-
D����0.2 mol��L��1��NH4Al(SO4)2��Һ��0.3 mol��L��1��Ba(OH)2��Һ�������ϣ�
2Al3����3SO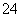 ��3Ba2����6OH��=2Al(OH)3����3BaSO4��
��3Ba2����6OH��=2Al(OH)3����3BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ�������£�ij��Ӧ�Ļ�ѧ����ʽΪ��CO2��NO  NO2��CO ������˵����ȷ���ǣ� ��
NO2��CO ������˵����ȷ���ǣ� ��
A�������¶ȣ�����Ӧ���������淴Ӧ���ʼ���
B������ʱ��ѹ���������������ɫ�����ƽ������
C���ﵽƽ�⣬��ƽ�ⳣ��Ϊ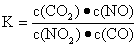
D������ʱ�������¶ȣ�����������ɫ����÷�Ӧ���ʱ�Ϊ��ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���������ܱ������г���H2��I2��������ӦH2 (g) + I2 (g) 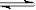 2HI(g) ��H<0��
2HI(g) ��H<0��
���ﵽƽ���t0ʱ�̸ı�ijһ������������������䣩��������ѹǿ����
����˵����ȷ����(����)
A������Ϊ���� B��ƽ��һ�����ƶ� C��H2 ת�������� D��HIƽ��Ũ��һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ����
��A��1molH2O��Լ����6.02��1023��H���� ��B��1molCH4�����ԼΪ22.4L
��C��CO2��Ħ������Ϊ44g�� �� D��1molNaOH������40g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ��������Ҫ����2 mol��L��1��NaCl��Һ950 mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ��NaCl�����ֱ���(����)
A��950 mL,111.2 g B��500 mL,117 g C��1 000 mL,117 g D��������111.2 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ��ijЩ���ӵļ��鼰����һ����ȷ����(���� )
A������ϡ���������ɫ���壬������ͨ�����ʯ��ˮ����Һ����ǣ�һ����CO32-
B�������Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42-
C����������ϡ���ᣬ�ټ����Ȼ�����Һ���а�ɫ����������һ����SO42-
D������̼������Һ������ɫ�������ټ����������ʧ��һ����Ba2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڷ�Ӧ3Cl2+6NaOH=NaClO3+5NaCl+3H2O�У�����m g C l2������ʱ������ԭ�������ǣ� ����
l2������ʱ������ԭ�������ǣ� ����
A��3m g B. 5m g C. 6m/35.5 mol D. 5m/71 mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com