
(1)原KI溶液的物质的量浓度。
(2)参加反应的Cl2有多少升(标准状况)?
(1)c(KI)=1 mol·L-1
(2)V(Cl2)=2.24 L
解析:(1)23.2 g固体为KCl与KI,含碘为27.32%,则含KI为
27.32%×![]() =35.7%
=35.7%
则m(KCl)=23.2 g×64.3%=14.9 g
参加反应的KI的物质的量为:
2KI + Cl2 ====2KCl+I2
2 mol 1mol 149 g
n′(KI)=0.2 mol 14.9 g
参加反应的Cl2为0.1 mol,标准状况下的体积为2.24 L
23.2 g固体中所含KI的质量为
23.2 g-14.9 g=8.3 g即0.05 mol
原KI溶液中的KI的物质的量浓度为:
c(KI)=![]() =1 mol·L-1
=1 mol·L-1
(2)参加反应的Cl2在标准状况下的体积为2.24 L。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
他们设计如下制取氯气并验证其性质的实验:

选用_________装置(填写装置的序号)制取氯气。
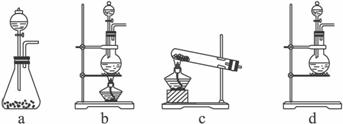
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已部分被氧化(简述实验步骤):
____________________________________________________________________
(3)写出在D装置中发生反应的离子方程式:______________________________________
(4)该实验存在明显的缺陷,请你提出改进的方法。
____________________________________________________________________
(5)该小组又进行了如下实验:称取漂白粉
查看答案和解析>>
科目:高中化学 来源: 题型:
用a mol H2与b mol Cl2合成HCl,再将反应后的气体通入足量的NaOH溶液中充分吸收,按要求填写下表(可不填满):
| a和b大小关系 | 通过NaOH溶液后是否有气体剩余及其质量 | 生成NaCl物质的量 |
①a=b 无 2a或2b mol
②a>b 2(a-b) mol H2 2b mol
③a<b 无 (a+b) mol
27.在250 mL KI溶液中通入一定量的Cl2,再将所得溶液蒸干,并加热到质量不再减少为止,称得固体质量为23.2 g,经实验分析所得固体中含碘27.32%,试计算:
(1)原KI溶液的物质的量浓度。
(2)参加反应的Cl2有多少升(标准状况)?
查看答案和解析>>
科目:高中化学 来源:2012届山东省济宁市邹城二中高三第二次质量检测化学试卷 题型:实验题
(14分)某研究性学生小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO42CaSO4+2Cl2↑+2H2O他们设计了如图所示装置制取氯气并验证其性质的实验。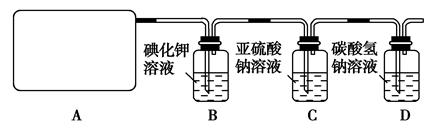
试回答:
(1)该实验中A部分的装置是________(填写装置的序号);
(2)B中反应的化学方程式是 。
(3)写出C中反应的离子方程式 ,并请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):_________________ 。
(4)写出在D装置中发生反应的离子方程式 。
(5)该实验存在明显的缺陷是__________________________________。
(6)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为2Na2S2O3+I2===Na2S4O6+2NaI,反应完成时,共消耗Na2S2O3 200 mL。则该漂白粉中Ca(ClO)2的质量分数为___ _____。
查看答案和解析>>
科目:高中化学 来源:2014届江苏省扬州市高二下学期期末调研测试化学试卷(解析版) 题型:实验题
碘溶于碘化钾溶液中形成I3—,并建立如下平衡:I3— I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
实验原理:
为了测定平衡时的c(I3—) ,可用过量的碘与碘化钾溶液一起摇动,达平衡后取上层清液用标准的Na2S2O3滴定:2 Na2S2O3 + I2 = 2NaI + Na2S4O6。
由于溶液中存在I3— I— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3—的总浓度,设为c1,c1 =
c(I2)+c(I3—);c(I2)
的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)=
c2,c(I3—)=c1 —c2;
I— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3—的总浓度,设为c1,c1 =
c(I2)+c(I3—);c(I2)
的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)=
c2,c(I3—)=c1 —c2;
实验内容:
1.用一只干燥的100 mL 碘量瓶和一只250 mL碘量瓶,分别标上1、2号,用量筒取80 mL 0.0100 mol.L-1 KI于1号瓶,取200 mL 蒸馏水于2号瓶,并分别加入0.5 g过量的碘。
2.将两只碘量瓶塞好塞子,振荡30分钟,静置。
3.分别取上层清液20 mL用浓度为c mol/L标准Na2S2O3溶液进行滴定。1号瓶消耗V1 mL Na2S2O3溶液,2号瓶消耗V2 mL Na2S2O3溶液。
4.带入数据计算c(I3—)
试回答下列问题
(1)标准Na2S2O3溶液应装入 (填“酸式滴定管”或“碱式滴定管”),原因是 。
(2)碘量瓶在震荡静置时要塞紧塞子,可能的原因是
(3)滴定时向待测液中加入的指示剂是 ,到达滴定终点时的现象为 。
(4)用c 、V1 和V2 表示c(I3—)为 mol·L-1。
(5)若在测定1号瓶时,取上层清液时不小心吸入了少量的I2固体,则测定的c(I3—) (填“偏大”、“偏小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com