
| A、SiO2是酸性氧化物,不与任何酸反应 |
| B、物质的量浓度相同的Na2SiO3和Na2CO3溶液,其PH值前者大于后者 |
| C、高温时SiO2和Na2CO3反应放出CO2,说明硅酸的酸性比碳酸强 |
| D、水玻璃敞口存放,会有沉淀析出 |


科目:高中化学 来源: 题型:
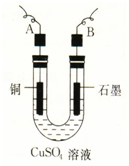 某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如图所示,回答下列问题:
某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4×l0-3 mol/L |
| B、2×l0-3 mol/L |
| C、1×l0-3 mol/L |
| D、1×l0-7 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、2:5 |
| C、3:7 | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6、C3H6、C4H6 |
| B、CH4、C2H4、C3H4 |
| C、C2H4、C3H6、C3H4 |
| D、CH4、C2H6、C3H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- | ||
B、常温下的溶液:
| ||
| C、O.1 mol/L AgNO3溶液:H+、K+、SO42-、I- | ||
| D、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 方案 | 操作过程 | 现象和结论 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O和Na2O2都是钠的氧化物,都是碱性氧化物 |
| B、Na2O和Na2O2它们都是白色固体 |
| C、Na2O2与二氧化碳的反应中,Na2O2既是氧化剂又是还原剂 |
| D、1mol Na2O2在和水的反应中,转移的电子数约为:1.204×1024个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com