
| 选项 | 实验操作 | 现象 | 结论 |
| A | CH2=CH2通入溴的四氯化碳溶液中 | 溶液褪色 | CH2=CH2发生取代反应 |
| B | KIO3溶液中加入HI溶液并加入淀粉 | 溶液变蓝色 | 氧化性:KIO3>I2 |
| C | 将盛满氯气的试管倒扣在水槽中,放在日光下静置一段时间 | 气体逐渐减少,最后变为无色 | Cl2置换出水中的氧生成了O2 |
| D | 将苯、溴水混合后加入大试管加热 | 试管底部产生油状物 | 苯发生取代反应生成溴苯 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溴和碳碳双键能发生加成反应;
B.氧化剂的氧化性大于氧化产物的氧化性;
C.氯气和水反应生成HCl和HClO,HClO不稳定,易分解生成氧气;
D.苯和液溴在溴化铁作催化剂条件下能反应生成溴苯,苯能萃取溴水中的溴.
解答 解:A.溴和碳碳双键能发生加成反应生成1,2-二溴乙烷,该反应是加成反应不是取代反应,故A错误;
B.氧化剂的氧化性大于氧化产物的氧化性,淀粉试液变蓝色,说明碘酸钾和HI发生氧化还原反应生成碘,碘酸钾中I元素化合价由+5价变为0价、HI中I元素化合价由-1价变为0价,所以碘酸钾是氧化剂、碘是氧化产物,则氧化性KIO3>I2,故B正确;
C.氯气和水反应生成HCl和HClO,HClO不稳定,易分解生成氧气,所以氧气是次氯酸分解得到的不是氯气和水发生置换反应得到的,故C错误;
D.苯和液溴在溴化铁作催化剂条件下能反应生成溴苯,苯能萃取溴水中的溴而使溴水褪色,苯密度小于溴,所以油状液体应该在试管上部,故D错误;
故选B.
点评 本题考查化学实验方案评价,侧重考查学生分析判断能力,涉及萃取、氧化还原反应、取代反应等知识点,明确物质性质是解本题关键,易错选项是C.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.
甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.| 化学键 | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ•mol-1 | a | b | c | d | e |
| 容器 | 反应物投入的量 | 反应物的转化率 | CH2OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1molCO和2molH2 | a1 | c1 | 放出Q1kJ热量 |
| 乙 | 1molCH3OH | a2 | c2 | 放出Q2kJ热量 |
| 丙 | 2molCO和4molH2 | a3 | c3 | 放出Q3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. (其中一种).
(其中一种). )的合成路线.
)的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | b电极上发生还原反应 | |
| B. | 外电路电子的流向是从a到b | |
| C. | 电池工作时,盐桥中的SO42-移向甲烧杯 | |
| D. | a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +nH2O.
+nH2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
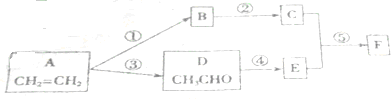

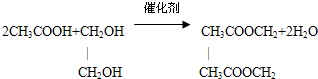 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为水分子间存在氢键,所有水分子较稳定 | |
| B. | 碘固体升华过程中吸收的热量用于克服碘原子间的作用力 | |
| C. | 溴化氢溶于水能电离出H+、Br-,所以溴化氢是离子化合物 | |
| D. | 纯碱和烧碱的熔化均破坏了离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com