
向Fe2(SO4)3、CuCl2混和溶液中投入足量的铁粉充分反应后,得到的固体经过滤、干燥、称重,剩余金属粉末的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比是 ( )
| A.3︰2 | B.1︰7 | C.2︰7 | D.1︰14 |
D
解析试题分析:设H2SO4物质的量为x,CuSO4物质的量为y.
Fe+H2SO4=FeSO4+H2↑ 固体减少质量△m
1 mol 56 g
x 56x
Fe+CuSO4=FeSO4+Cu 固体增加质量△m
56 1mol 64 8g
y 8y
充分反应后,剩余金属粉末的质量与原加入铁粉的质量相等,所以56x=8y,即x/y=1/7,
则原溶液中H+和SO42-的物质的量浓度之比=2x/(x+y)=1/4。故选D。
考点:铁的化学性质 化学方程式的有关计算
点评:本题考查了金属活动性顺序的应用以及根据反应的化学方程式的计算,完成此题,关键是抓住题干提供的剩余固体物质的质量与所加铁粉的质量相待,巧妙利用固体质量差量法进行计算。


科目:高中化学 来源: 题型:
A.向氢氧化钠溶液中通入少量CO2
![]()
![]()
B.用氨水吸收少量SO2
2NH3·H2O+SO2![]() 2
2![]() +
+ ![]() +H2O
+H2O
C.硝酸铝溶液中加入过量氨水
Al3++4NH3·H2O![]()
![]() +4
+4![]() +2H2O
+2H2O
D.向Fe2(SO4)3的酸性溶液中通入足量H2S
Fe3++H2S![]() Fe2++S↓+2H+
Fe2++S↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A.向氢氧化钠溶液中通入少量CO2
OH-+CO2===HCO![]()
B.用氨水吸收少量SO2
2NH3·H2O+SO2===2NH![]() +SO
+SO![]() +H2O
+H2O
C.硝酸铝溶液中加入过量氨水
Al3++4NH3·H2O===AlO![]() +4NH
+4NH![]() +2H2O
+2H2O
D.向Fe2(SO4)3的酸性溶液中通入足量H2S
Fe3++H2S===Fe2++S↓+2H+
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省孝感市三年级第一次统一考试化学试卷(解析版) 题型:填空题
二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质)。某课题以此粉末为原料,资源回收的工艺流程如下:
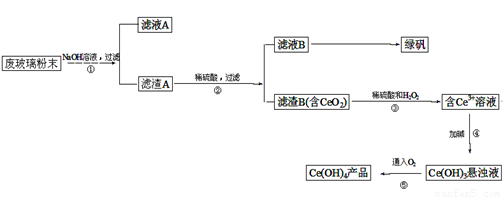
(1)写出第①步反应的离子方程式 。
(2)洗涤滤渣B的目的是为了除去____(填离子符号),检验该离子是否洗净的方法是 。
(3)写出第③步反应的化学方程式_____________________________。
(4)制备绿矾(FeSO4·7H2O)时,向Fe2(SO4)3溶液中加入过量铁屑,充分反应后,经过滤得到FeSO4溶液,再经 、 、过滤、洗涤、干燥等操作步骤得到绿矾。
(5)取上述流程中得到的Ce(OH)4产品(质量分数为97%)1.0g,加硫酸溶解后,用0.1000mol/LFeSO4溶液滴定至终点(铈被还原成Ce3+),则需准确滴加标准溶液的体积为 mL。
查看答案和解析>>
科目:高中化学 来源:2015届湖北武汉部分重点中学高一上学期期末考试化学试卷(解析版) 题型:选择题
向Fe2(SO4)3、CuCl2混和溶液中投入足量的铁粉充分反应后,得到的固体经过滤、干燥、称重,剩余金属粉末的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比是 ( )
A.3︰2 B.1︰7 C.2︰7 D.1︰14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com