
| ||
| ||
| ||
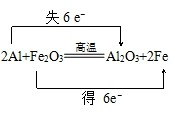 ,
, ;Fe2O3;Al;3;
;Fe2O3;Al;3;

 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
| A、Na2SO4 |
| B、CH3COOH |
| C、NaOH |
| D、CH3COOK |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于磷化氢的相对分子质量比氨气的大,所以沸点:PH3>NH3 |
| C、若A2+2D-═2A-+D2,则氧化性D2>A2 |
| D、若R2-和M+的电子层结构相同,则离子半径R2->M+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
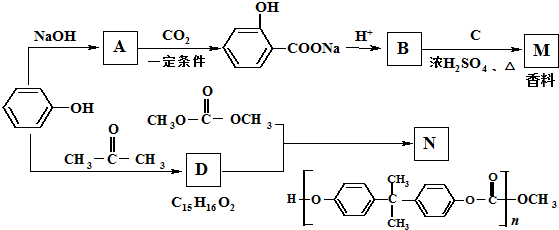
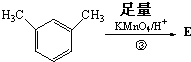 其中核磁共振氢谱显示其分子中含有4种不同的氢原子的为
其中核磁共振氢谱显示其分子中含有4种不同的氢原子的为查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCN |
| 醇溶液 |
| H2O |
| H2SO4 |
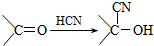
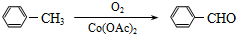
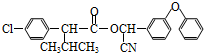 ):
):
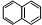 )的一取代物,含有碳碳叁键,X所有可能的结构共有
)的一取代物,含有碳碳叁键,X所有可能的结构共有查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 电离常数Ka |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| CH3COOH | Ka=1.8×10-5 |
| HClO | Ka=3.0×10-8 |
| A、pH相同的Na2CO3、CH3COONa、NaClO各加水稀释相同倍数,pH变化最小的是Na2CO3 |
| B、表中所列的三种酸的溶液中滴入石蕊试剂,溶液一定都变红 |
| C、次氯酸钠溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=CO32-+2HClO |
| D、常温下,在0.1mol/L的CH3COOH溶液中滴加0.1mol/L的NaOH溶液发生反应,当c(H+)=1.8×10-5时,溶液中下列微粒的浓度大小关系为:c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
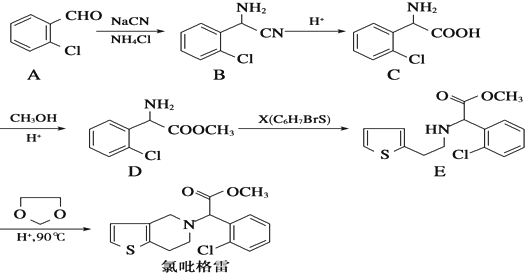
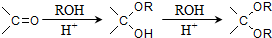
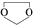 ,需要经历的反应类型有
,需要经历的反应类型有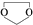 的最后一步反应
的最后一步反应查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PCl3与PCl5 |
| B、PCl3 |
| C、PCl5 |
| D、无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com