
| A��2 Fe3++2 I-��2 Fe2++I2 |
| B��2 NO3-+6 I-+8 H+��2 NO��+3 I2+4 H2O |
| C��5 NO3-+Fe3++16 I-+20 H+��Fe2++5 NO��+8 I2+10 H2O |
| D��2 NO3-+4 Fe3++10 I-+8 H+��4 Fe2++2 NO��+5 I2+4 H2O |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��֪ | ���� | |||||||||
| A | ��Fe����CuSO4��Һ�У�Fe+Cu2+=Cu+Fe2+ | ��Na���뵽CuSO4��Һ�У�2Na+Cu2+=Cu+2Na+ | ||||||||
| B | ϡ������Ba��OH��2��Һ��Ӧ����Һ�����ԣ�2H++SO42-+Ba++2OH-=BaSO4��+2H2O | NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����ԣ�2H++SO42-+Ba++2OH-=BaSO4��+2H2O | ||||||||
| C | ����������Ӧ2Fe+3Cl2
|
���͵��ʷ�Ӧ2Fe+3I2
| ||||||||
| D | ��Ca��ClO��2��Һ��ͨ������CO2��Ca2++2ClO-+CO2+H2O=CaCO3��+2HClO | ��Ca��ClO��2��Һ��ͨ������SO2��Ca2++2ClO-+SO2+H2O=CaSO3��+2HClO |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �������ϰ�װ��ת������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯������Ӧ�����������ʣ���������β����Ⱦ��
�������ϰ�װ��ת������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯������Ӧ�����������ʣ���������β����Ⱦ��
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c��NO�� ����10-4mol?L-1�� |
10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c��CO�� ����10-3mol?L-1�� |
3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
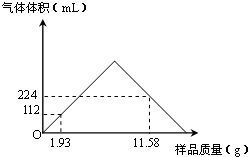 ������������ʵ���Һ�ҵ�����ж��й㷺����;��
������������ʵ���Һ�ҵ�����ж��й㷺����;��| 500-520�� |
| 1 |
| 9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�22.4LO2��N2�Ļ�������з�������ΪNA |
| B�����³�ѹ�£�1molI2�����У�����Iԭ����Ϊ2NA |
| C��Na2O2��H2O��Ӧ����16gO2ʱ��ת�Ƶ�����ΪNA |
| D����״���£���������ΪNA��H2��H2O��������ռ�������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ũ��Ϊ0.1mol?L-1 HF��Һ��ˮ����ϡ�����У�c�� H+�� ��c �� OH-�������С |
| B��Ϊȷ��ij��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��PH����PH��7����H2A�������PH��7����H2A��ǿ�� |
| C����SO2ͨ��һ����KOH��Һ��������Һ�����ԣ�����Һ��һ����KHSO3 |
| D����0.200mol?L-1 NaOH����Һ�ζ�Ũ�Ⱦ�Ϊ0.1mol?L-1 ��HCl��CH3COOH�Ļ��Һ��������ʱ����Һ�е���ǡ�ñ���ȫ�к� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������[KAl��SO4��2]��Һ����μ���Ba��OH��2��Һ��SO4-ǡ�ó�����ȫ��2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4 |
| B����ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+Fe��OH��3�TFeO42-+3Cl-+H2O+H+ |
| C����NaAlO2��Һ��ͨ�����CO2��Al��OH��3��2AlO2-+CO2+3H2O�T2Al��OH��3��+CO |
| D��Ca��HCO3��2�����Ca��OH��2��Һ��Ӧ��Ca2++HCO3++OH-�TCaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com