
 2NH3(g)””¦¤H<0µÄĖŁ¶ČĪŖv£¬Čō½µµĶĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼Ó“ó
2NH3(g)””¦¤H<0µÄĖŁ¶ČĪŖv£¬Čō½µµĶĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼Ó“ó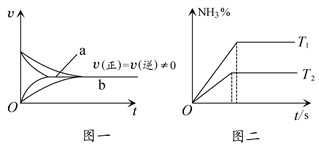
| A£®³ż¢Ł¢ßĶā | B£®³ż¢Ū¢Ż¢ŽĶā | C£®³ż¢Ū¢ŻĶā | D£®³ż¢Ū¢Ž¢ßĶā |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ū¢Ü | B£®¢Ł¢Ś¢Ü | C£®¢Ł¢Ś¢Ū¢Ü | D£®¢Ł¢Ś¢Ū¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| ””””””””””””ŹµŃé »ģŗĻČÜŅŗ”””””””””” | A | B | C | D | E | F |
| 4 mol”¤L-1 H2SO4ČÜŅŗ/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| ±„ŗĶCuSO4ČÜŅŗ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| ×鱚 | c(HCl)/mol”¤L-1 | ĪĀ¶Č/”ę | דĢ¬ |
| 1 | 2.0 | 25 | æéד |
| 2 | 2.5 | 30 | æéד |
| 3 | 2.5 | 50 | æéד |
| 4 | 2.5 | 50 | ·Ūĩד |
 3
3 2
2 1 B.1
1 B.1 2
2 3
3 4 C.3
4 C.3 4
4 2
2 1 D.1
1 D.1 2
2 4
4 3
3²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĪĀ¶ČŌ½øߣ¬“߻ƼĮµÄ“߻Ɗ§¹ūŌ½ŗĆ |
| B£®Ęū³µÅÅĘų¹ÜÉĻµÄ”°“ß»Æ×Ŗ»ÆĘ÷”±ÄܼõÉŁÓŠŗ¦ĘųĢåÅÅ·Å |
| C£®“߻ƼĮæÉŅŌøıä»Æѧ·“Ó¦ĖŁĀŹ£¬µ«·“Ó¦Ē°ŗóÖŹĮæŗĶ»ÆѧŠŌÖŹ²»±ä |
| D£®ŠæÓėŃĪĖį·“Ó¦Ź±£¬¼ÓČė¼øµĪĮņĖįĶČÜŅŗæɼÓæģ·“Ó¦ĖŁĀŹ£¬µ«ĮņĖįĶ²»×÷“߻ƼĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
| ·“Ó¦½ų³Ģ (·ÖÖÓ) | 1 | 2 | 5 | 15 | 20 |
| 4.0 mol/L ŃĪĖį | ÉŁĮæĘųÅŻ | ½Ļ¶ąĘųÅŻ | “óĮæĘųÅŻ | ·“Ó¦¾ēĮŅ | ĀĮʬŗľ” |
| 2.0 mol/L ĮņĖį | ĪŽĆ÷ĻŌĻÖĻó | ¼«ÉŁĮæ ĘųÅŻ | ÉŁĮæĘųÅŻ | ||
| 4.0 mol/L ĮņĖį | ĪŽĆ÷ĻŌĻÖĻó | ÉŁĮæĘųÅŻ | ÓŠ±Č½ĻĮ¬ŠųµÄĘųÅŻ | ||
| ŹµŃéÄæµÄ | ŹµŃé ±ąŗÅ | ĪĀ¶Č /”ę | ½šŹōĀĮµÄ ŠĪĢ¬ | ŃĪĖįÅØ¶Č /mol”¤L£1 |
| 1.ŹµŃé¢ŁŗĶ¢ŚĢ½¾æŃĪĖįÅØ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£» 2£®ŹµŃé¢ŁŗĶ¢ŪĢ½¾æĪĀ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£» 3£®ŹµŃé¢ŁŗĶ¢ÜĢ½¾æ½šŹō¹ęøń(ĀĮʬ”¢ ĀĮ·Ū)¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ | ¢Ł | 25 | ĀĮʬ | 4.0 |
| ¢Ś | | | | |
| ¢Ū | | | | |
| ¢Ü | | | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2SO3ŹĒÉś²ś¹ż³ĢÖŠµÄÖŲŅŖ·“Ó¦”£ĻĀĮŠ¶ŌÓŚøĆ·“Ó¦µÄĖµ·ØÖŠÕżČ·µÄŹĒ
2SO3ŹĒÉś²ś¹ż³ĢÖŠµÄÖŲŅŖ·“Ó¦”£ĻĀĮŠ¶ŌÓŚøĆ·“Ó¦µÄĖµ·ØÖŠÕżČ·µÄŹĒ| A£®Ö»ŅŖŃ”ŌńŹŹŅĖµÄĢõ¼ž£¬SO2ŗĶO2¾ĶÄÜČ«²æ×Ŗ»ÆĪŖSO3 |
| B£®øĆ·“Ó¦“ļµ½Ę½ŗāŗ󣬷“Ó¦¾ĶĶźČ«Ķ£Ö¹ĮĖ£¬¼“ÕżÄę·“Ó¦ĖŁĀŹ¾łĪŖĮć |
| C£®Čē¹ū·“Ó¦Ē°³äČėÓÉ18OŌ×Ó×é³ÉµÄO2£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬18OÖ»“ęŌŚÓŚO2ŗĶSO3ÖŠ |
| D£®ŌŚ¹¤ŅµŗĻ³ÉSO3Ź±£¬ŅŖĶ¬Ź±æ¼ĀĒ·“Ó¦ĖŁĀŹŗĶ·“Ó¦ÄÜ“ļµ½µÄĻŽ¶ČĮ½·½ĆęµÄĪŹĢā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
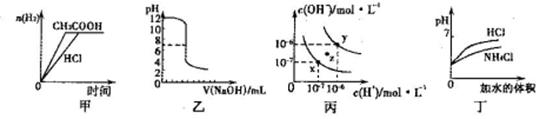
| A£®¼×Ķ¼ĒśĻß±ķŹ¾ĻņµČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄŃĪĖįŗĶ“×ĖįČÜŅŗÖŠ·Ö±š¼ÓČĖ×ćĮæĆ¾·Ū²śÉśH2µÄĪļÖŹµÄĮæµÄ±ä»Æ |
| B£®ŅŅ±ķŹ¾½«0.01mol”¤L-lNaOHČÜŅŗµĪČĖµ½Ļ”ŃĪĖįÖŠµÄµĪ¶ØĒśĻß |
| C£®±ūĪŖĖ®µÄµēĄėĒśĻߣ¬“ÓzµćŲŁxµć£¬æɲÉÓĆŌŚĖ®ÖŠ¼ÓČėŹŹĮæNaOH¹ĢĢåµÄ·½·Ø |
| D£®¶”ÖŠĒśĻß±ķŹ¾½«pHĻąĶ¬µÄNH4C1ČÜŅŗŗĶŃĪĖįĻ”ŹĶĻąĶ¬±¶ŹżŹ±£¬¶žÕßpHµÄ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

A£®N2(g)+3H2(g) 2NH3(g) ¦¤H=£Q1 kJ”¤mol-1(Q1£¾0)”” 2NH3(g) ¦¤H=£Q1 kJ”¤mol-1(Q1£¾0)”” |
B£®2SO3(g) 2SO2(g)+O2(g) ¦¤H=+Q2 kJ”¤mol-1(Q2£¾0) 2SO2(g)+O2(g) ¦¤H=+Q2 kJ”¤mol-1(Q2£¾0) |
C£®4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ¦¤H=£Q3 kJ”¤mol-1(Q3£¾0) 4NO(g)+6H2O(g) ¦¤H=£Q3 kJ”¤mol-1(Q3£¾0) |
D£®H2(g)+CO(g) C(s)+H2O(g) ¦¤H=+Q4 kJ”¤mol-1(Q4£¾0) C(s)+H2O(g) ¦¤H=+Q4 kJ”¤mol-1(Q4£¾0) |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com