
���� X��Y��Z��W��R��QΪǰ30��Ԫ�أ���ԭ��������������X������Ԫ����ԭ�Ӱ뾶��С�ģ���XΪHԪ�أ�Y�������ܼ�����ÿ���ܼ��ϵĵ�������ȣ���������Ų�Ϊ1s22s22p2����YΪCԪ�أ�R��Yͬһ���壬���ԭ��������֪��RΪSi����Zԭ�ӵ���������ͬ����Ԫ������࣬����Χ�����Ų�Ϊns2np3��ԭ������С��Si����ZΪNԪ�أ�W��Zͬ���ڣ���һ�����ܱ�Z�ĵͣ���WΪOԪ�أ�Q�������ֻ��һ�����ӣ��������Ӳ���Ӿ����ڱ���״̬��������Ϊ������Ԫ�أ�ԭ������С��30���ʺ�������Ų�Ϊ1s22s22p63s23p63d104s1����QΪCuԪ�أ��ݴ˽��
��� �⣺X��Y��Z��W��R��QΪǰ30��Ԫ�أ���ԭ��������������X������Ԫ����ԭ�Ӱ뾶��С�ģ���XΪHԪ�أ�Y�������ܼ�����ÿ���ܼ��ϵĵ�������ȣ���������Ų�Ϊ1s22s22p2����YΪCԪ�أ�R��Yͬһ���壬���ԭ��������֪��RΪSi����Zԭ�ӵ���������ͬ����Ԫ������࣬����Χ�����Ų�Ϊns2np3��ԭ������С��Si����ZΪNԪ�أ�W��Zͬ���ڣ���һ�����ܱ�Z�ĵͣ���WΪOԪ�أ�Q�������ֻ��һ�����ӣ��������Ӳ���Ӿ����ڱ���״̬��������Ϊ������Ԫ�أ�ԭ������С��30���ʺ�������Ų�Ϊ1s22s22p63s23p63d104s1����QΪCuԪ�أ�
��1��Q+ΪCu+��Cu+�����������Ϊ29����������Ų�ʽΪ��1s22s22p63s23p63d10��
�ʴ�Ϊ��1s22s22p63s23p63d10��
��2��������H2O2�нṹʽΪH-O-O-H��Oԭ�Ӽ۲���Ӷ���=2+$\frac{6-2}{2}$=4����Oԭ�Ӳ�ȡsp3�ӻ���
NO2-������Nԭ�ӹµ��Ӷ���Ϊ��$\frac{5+1-2��2}{2}$=1���۲���Ӷ���Ϊ2+1=3���������幹����V�Σ�
�ʴ�Ϊ��sp3��V�Σ�
��3��Y��R�����������ֱ�Ϊ������̼���������裬SiO2Ϊԭ�Ӿ��壬CO2Ϊ���Ӿ��壬�ʷе�ϸߵ��� SiO2��
�ʴ�Ϊ��SiO2��
��4����Cu���ʵķ�ĩ���뵽NH3��Ũ��Һ�У���ͨ��O2����ַ�Ӧ����Һ������ɫ����Ӧ����[Cu��NH3��4]2+���÷�Ӧ�����ӷ���ʽΪ��2Cu+8NH3+O2+2H2O=2[Cu��NH3��4]2++4OH-��
�ʴ�Ϊ��2Cu+8NH3+O2+2H2O=2[Cu��NH3��4]2++4OH-��
���� ����λ�ýṹ�����ʹ�ϵ��Ӧ�ã��漰��������Ų����ӻ���������ӹ���������֪ʶ����Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ŵ�ʱ����������pH���� | |
| B�� | �ŵ�ʱ�������ĵ缫��ӦʽΪPbO4+4H++2e-�TPb2++2H2O | |
| C�� | ���ʱ��Ǧ�缫���Դ���������� | |
| D�� | ���ʱ������������20.7g Pbʱ��Һ����0.2mol����ͨ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | b g | B�� | $\frac{3b}{4}$g | C�� | $\frac{b}{2}$g | D�� | $\frac{b}{4}$g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100ml 0.1mol/L����ˮ��ͨ��0.01molSO2���� | |
| B�� | 100ml 0.5mol/L��NaOH��ͨ��0.005mol���� | |
| C�� | 100ml 0.5mol/L��CuSO4��Һ�м���4g NaOH���� | |
| D�� | 100ml����ˮ�м���0.01mol�����ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
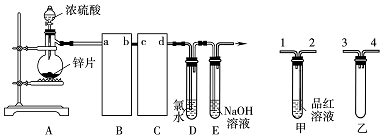
 ��ͼ��ʾʵ��װ�ÿ�������ȡ��Ȳ������գ�
��ͼ��ʾʵ��װ�ÿ�������ȡ��Ȳ������գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ս�����ƿ������������ζ | |
| B�� | Բ����ƿ�����þƾ���ֱ�Ӽ��� | |
| C�� | �������Ż�ʱ����ɳ������ | |
| D�� | Ũ����մ��Ƥ���ϣ�������������Һ��ϴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Խ��������ԽС�����ۻ�����Խ�ȶ� | |
| B�� | ͨ����Ӧ�������������м������ݿ��Դ���Ԥ�ⷴӦ�ȵĴ�С | |
| C�� | ������ȷ�����������ṹ��������״������Ҫ���� | |
| D�� | ͬ��ԭ�Ӽ��γɵĹ��ۼ���������������ѭ��������˫�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com