
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
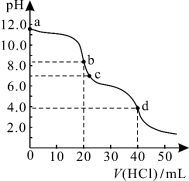
A.a点溶液呈碱性的原因用离子方程式表示为:CO +2H2O
+2H2O H2CO3+2OH-
H2CO3+2OH-
B.c点处的溶液中c(Na+)-c(Cl-)=c(HCO )+2c(CO
)+2c(CO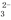 )
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
科目:高中化学 来源:2016-2017学年广西省高一上模拟考试化学卷(解析版) 题型:计算题
将0.1molMg 、Al混合物溶于100mL3mol/LHCl中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
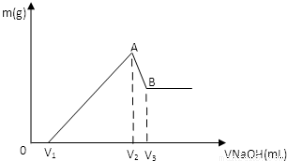
(1)写出A→B段反应的离子方程式  。
。
(2)A点沉淀的总物质的量n= 。
(3)欲使Mg2+ 、Al3+刚好沉淀完全,则加入NaOH溶液的体积为多少mL?(写出计算过程,下同)
(4)若V1=60mL,则混合物中Mg的物质的量为多少? V3点所加NaOH溶液的体积为多少mL?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,已知X的原子序数比Y的原子序数大,下列说法中正确的是
A. X的金属性比Y的金属性强
B. X和Y都不能从水中置换出氢
C. Y元素的氢氧化物碱性比X元素的氢氧化物碱性弱
D. X元素的最高化合价比Y元素的最高化合价高
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4 L H2O含有的分子数为NA
B.常温常压下, 1
1 .06 g Na2CO3含有的Na+离子数为0.02 NA
.06 g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,NA个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:推断题
[化学—选修5:有机化学基础]缩醛在有机合成中常用于保护羰基或作为合成中间体,同时还是一类重要的香料,广泛应用于化妆品、食物、饮料等行业。G是一种常用的缩醛,分子中含有一个六元环和一个五元环结构。下面是G的一种合成路线:
已知:
① 芳香烃A含氢元素的质量分数为8.7%,A的质谱图中,分子离子峰对应的最大质荷比为92;D的产量可以用来衡量一个国家的石油化工发展水平。
② 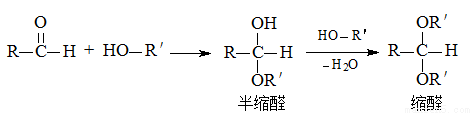
③ 同一个碳原子连接两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的结构简式是 ,E的名称是 。
(2)由D生成E的反应类型是 ,E→F的反应条件是 。
(3)由B生成N的化学方程式为 。
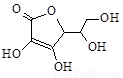
(4)有研究发现,维生素C可以作为合成G物质的催化剂,具有价廉、效率高、污染物少的优点。维生素C的结构如右图。则维生素C分子中含氧官能团名称为 。
(5)缩醛G的结构简式为 。G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式: 。
①既能发生银镜反应,又能与FeCl3发生显色反应;②核磁共振氢谱为4组峰。
(6)写出用2-丁烯为原料(其他无机试剂任选)制备顺丁橡胶(顺式聚1, 3-丁二烯)的合成路线: 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:选择题
下列关于常见有机物的说法正确的是
A.乙醚和乙醇互为同分异构体
B.糖类、油脂、蛋白质均能发生水解反应
C.聚氯乙烯可用作生产食品包装材料的原料
D.分子式为C3H8O的有机物,只有2种能发生酯化反应
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
向1 L的密闭容器中加入1 mol X、0.3 mol Z和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
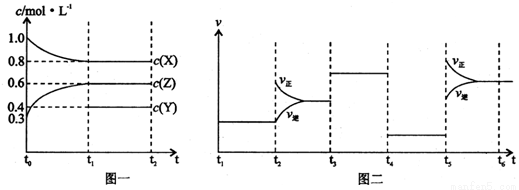
A.Y的起始物质的量为0.5 mol
B.该反应的化学方程式为:2X(g)+Y(g)  3Z(g) ∆H<0
3Z(g) ∆H<0
C.若t0=0,t1=10 s,则t0~t1 阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
D.反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源:2017届四川省资阳市高三第二次诊断性考试化学试卷(解析版) 题型:实验题
工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)制备铁红(Fe2O3)的生产流程如下:

试回答下列问题:
(1)步骤Ⅰ所得溶液中铁元素的化合价是 。
(2)实验室中实现步骤Ⅱ中分离操作需要的仪器有 、铁架台、玻璃棒、烧杯。
(3)步骤Ⅲ中发生的离子方程式 ,向反应后的溶液中加入试剂 ,当观察到 说明步骤Ⅲ已经进行完全。
(4)步骤Ⅳ中不能选用试剂 调节溶液的pH(填字母编号)。
a.FeO固体 b.氢氧化钠溶液 c.Fe2O3固体 d.氨水
(5)室温下FeCO3达到溶解平 衡时溶液pH=8.5,c(Fe2+)=1.2×10-6 mol·L-1。则FeCO3固体产物中 (选填“有”或“无”)Fe(OH)2。(已知:Ksp[Fe(OH)2]=4.8×10-16)
衡时溶液pH=8.5,c(Fe2+)=1.2×10-6 mol·L-1。则FeCO3固体产物中 (选填“有”或“无”)Fe(OH)2。(已知:Ksp[Fe(OH)2]=4.8×10-16)
(6)步骤Ⅵ中发生反应的化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省定西市通渭县高二上学期期末化学试卷(解析版) 题型:选择题
已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH。下列说法不正确的是( )
A.浓度均为0.1mol·L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强
B.0.1m ol·L-1CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
ol·L-1CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
C.NaF溶液中含有Na+、F-、H+、OH-、H2O、HF六种微粒
D.NaF溶液中加入少量NaOH固体,溶液中c(F-)变大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com