
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
【答案】A
【解析】A.Fe2O3溶于过量氢碘酸溶液中的离子反应为Fe2O3+6H++2I-═2Fe2++I2+3H2O,故A正确;B.0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合的离子反应为2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+2BaSO4↓+NH3.H2O,故B错误;C.0.1 mol·L-1的NaHA溶液pH=1,说明NaHA为强酸的酸式盐,HA-能完全电离出H+,则此反应的离子方程式为H++OH-=A2-+H2O,故C错误;D.向次氯酸钠溶液中通入足量SO2气体的离子反应为ClO-+SO2+H2O═2H++Cl-+SO42-,故D错误;故选A。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学欲除去固态氯化钠中混有的氯化钙。请根据如下实验方案回答相关问题:
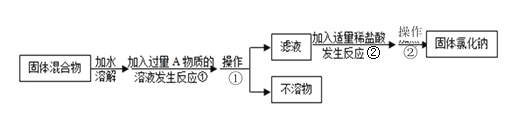
(1)操作①所需主要玻璃仪器有_________________________
(2)反应①中加入略过量的A物质的目的是______________________;判断A已过量的实验操作方法是_______________________________________________;反应①的化学反应方程式为___________________________________________________。
(3)操作②的名称为__________________;反应②的离子方程式______________________。
(4)实验时称取样品质量为185.0g,经过操作①后,经洗涤、干燥后测得沉淀质量为50.0g,则样品中NaCl的质量百分数为_________________________。(保留到小数点后第一位)
查看答案和解析>>
科目:高中化学 来源: 题型:
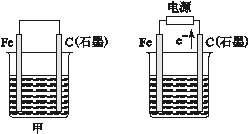
【题目】如图所示甲、乙是电化学实验装置:
 乙
乙
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为_________________________________________________。
②乙中总反应的离子方程式为___________________________________________________。
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为_____。
(2))若甲、乙两烧杯中均盛有CuSO4溶液:
①甲中铁棒上的电极反应式为___________________________________________________。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入_____________________(填写物质的化学式)______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应均为放热反应,其中反应热最小的是
A.2A(l) + B(l) = 2C (g) △H1
B.2A(g) + B(g) = 2C(g) △H2
C.2A (g) + B ( g ) = 2C(l) △H3
D.2A (l) + B(l)= 2C(l) △H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关SO3的说法中正确的是( )
A. 标准状况下,1molSO3的体积约为22.4L
B. SO3极易溶于水,且与水反应生成H2SO4
C. 将SO3加入BaCl2溶液无明显现象
D. SO2和SO3均具有漂白性,能使紫色石蕊溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种有机物Q(![]() )与P(
)与P(![]() ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )
A. 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶2
B. 二者在NaOH醇溶液中均可发生消去反应
C. 一定条件下,二者在NaOH溶液中均可发生取代反应
D. Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应X(g)+3Y(g)![]() 2Z(g);ΔH<0 在不同温度、不同压强(P1>P2)下,达到平衡时,混合气体中Z的体积分数φ(Z)随温度变化的曲线为 ( )
2Z(g);ΔH<0 在不同温度、不同压强(P1>P2)下,达到平衡时,混合气体中Z的体积分数φ(Z)随温度变化的曲线为 ( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通电条件下,用如图所示装置由乙二醛(OHC-CHO)制备乙二酸(H00C-COOH)。其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl。下列说法正确的是

A. 每消耗0.1mol乙二醛在Pt1极放出2.24L气体(标准状况)
B. Pt1的电极反应为:4OH--4e-=2H2O+O2↑
C. 每得到lmol乙二酸将有2molH+从右室迁移到左室
D. 盐酸是起提供Cl-和增强导电性的作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com