
将等物质的量的A、B混合于2L密闭容器中发生如下反应:3A(g)+B(g) 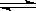 xC(g)+2D(g),4min时测得D的浓度为0.4mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min),列式计算:
xC(g)+2D(g),4min时测得D的浓度为0.4mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min),列式计算:
(1)x=__________;
(2)B在这4min内的平均反应速率__________;
(3)此时A的浓度及反应开始前容器中A、B的物质的量__________。
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源:2015-2016学年江西省高二下期末化学试卷(解析版) 题型:实验题
正丁醇常用作有机反应的溶剂。实验室制备正丁醇的主要实验装置如下图:

反应物和产物的相关数据如下下:
相对分 子质量 | 沸点/ ℃ | 密度 (g•cm-3) | 水中溶解性 | |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成正丁醚的步骤:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间,分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70mL水的分液漏斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚13g.
请回答:
(1)加热A前,需先从_______________b(填“a”或“b”)口向B中通入水;
(2)步骤①中浓硫酸和正丁醇的添加顺序为_______________;写出步骤②中制备正丁醚的化学方程式_______________;
(3)步骤③的目的是初步洗去________,振摇后静置,粗产物应从分液漏斗的_____上(填“上”或“下”)口分离出;
(4)步骤④中最后一次水洗的目的为_______________;
(5)步骤⑤中,加热蒸馏时应收集______(填选项字母)左右的馏分;
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为_________,下层液体的主要成分为_______________(填物质名称);
(7)本实验中,正丁醚的产率为_______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期末化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列有关说法错误的是
A.油脂和蛋白质都属于高分子化合物
B.乙醇室温下在水中的溶解度大于溴乙烷
C.以液化石油气代替燃油可减少大气污染
D.“地沟油”禁止食用,但可以用来制皂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津一中高二下期末化学试卷(解析版) 题型:选择题
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为:CH2=C=O+HA→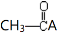 。乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
。乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
A.与 HCl 加成生成 CH3COCl
B.与 H2O加成生成 CH3COOH
C.与 CH3OH 加成生成 CH3COCH2OH
D.与 CH3COOH加成生成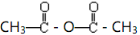
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津一中高二下期末化学试卷(解析版) 题型:选择题
如图是常见四种有机物的比例模型示意图。下列说法正确的是
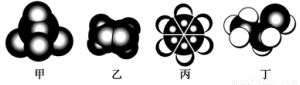
A.甲能使酸性高锰酸钾溶液褪色
B.乙可与溴水发生取代反应使溴水褪色
C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键
D.丁在稀硫酸作用下可与乙酸发生取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期末化学试卷(解析版) 题型:选择题
“低碳经济,节能减排”是21世纪世界经济发展的新思路。下列与之相悖的是( )
A.开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
C.大力开采煤、石油和天然气,以满足经济发展的需要
D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期末化学试卷(解析版) 题型:选择题
2011年中国已超北美成为全球液晶显示器第二大市场。生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
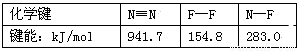
下列说法中不正确的是 ( )
A.过程F2(g)→2F(g)吸收能量
B.过程N(g)+3F(g)→NF3(g)放出能量
C.反应N2(g)+3F2(g)=2NF3(g)的ΔH<0
D.NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二下期末化学试卷(解析版) 题型:选择题
Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物。其漂白原理可用下面的反应方程式表示:

下列说法正确的是
A.品红溶液中同时通入Cl2、SO2,漂白效果会更好
B.加热不能判断品红褪色是通入SO2还是通入Cl2引起的
C.“无色化合物”分子中,19个碳原子都可能在同一平面上
D.品红分子结构中,19个碳原子都可能在同一平面上
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:推断题
物质X是某新型净水剂的中间体,它可以看成由氯化铝(在180℃升华)和一种盐A按物质的量之比1:2组成。在密闭容器中加热8.75g X使之完全分解,冷却后可得到3.2 g固体氧化物B、0.448L无色气体D(体积已折算为标准状况)、4.27g混合晶体E。B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色。D气体能使品红褪色。请回答下列问题:
(1)X的化学式为 。
(2)将A固体隔绝空气充分灼烧,使其分解,生成等物质的量的B、D和另一种化合物,则A分解的化学方程式为 。
(3)将E混合晶体溶于水配成溶液,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为 。E混合晶体中某种物质在一定条件下能和KI固体反应,写出该方程式 。
(4)高温下,若在密闭容器中长时间煅烧X,产物中还有另外一种气体,其分子式是 。请设计实验方案验证之 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com