
人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用.粗盐中含有Ca2+、Mg2+、SO42﹣以及泥沙等杂质,请回答粗盐提纯的有关问题:
(1)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤ .请补全实验步骤,并回答步骤③的目的 .
(2)2010年7月26日,卫生部公布了《食用盐碘含量》的征求意见稿,面向社会征求意见.对于食用盐中碘含量平均水平的规定有所降低.食盐中添加的是KIO3.可用下列反应来检验食
盐中是否含KIO3:KIO3+KI+H2SO4﹣I2+K2SO4+H2O (未配平).请配平该反应并表示出电子转移的方向和数目 ;为了获取反应后溶液中的I2,可采取的实验操作方法的名称是 .
考点: 物质的分离、提纯的基本方法选择与应用;氧化还原反应的电子转移数目计算.
分析: (1)在粗盐提纯时,要在最后一步加入盐酸,除去过量的氢氧根离子和碳酸根离子,加入碳酸钠的目的是除去钙离子和多余的钡离子;
(2)氧化还原反应中,化合价升高值=化合价降低值=转移电子数,根据化合价的升降情况来分析,碘单质从碘水中提取可以采用萃取分液法.
解答: 解:(1)在粗盐提纯时,要在最后一步加入盐酸,除去过量的氢氧根离子和碳酸根离子,因加入过量氯化钡,加入碳酸钠的目的是除去钙离子和多余的钡离子,
故答案为:加适量盐酸; 除去Ca2+及过量Ba2+;
(2)根据电子守恒和原子守恒来配平方程式,在氧化还原反应KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O中,化合价升高值=化合价降低值=转移电子数=6,电子转移情况如下: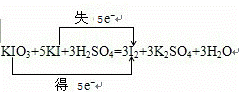 ,碘单质从碘水中提取可以采用萃取分液法,利用四氯化碳来萃取,然后根据四氯化碳和碘的沸点的不同来分离,
,碘单质从碘水中提取可以采用萃取分液法,利用四氯化碳来萃取,然后根据四氯化碳和碘的沸点的不同来分离,
故答案为: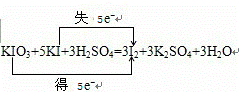 ;萃取、蒸馏.
;萃取、蒸馏.
点评: 本题综合考查物质的分离、提纯以及氧化还原反应,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握除杂的原理和操作方法,从化合价的角度认识氧化还原反应,难度不大.


科目:高中化学 来源: 题型:
下列反应中铁元素被还原的是()
A. 2Fe(OH)3 Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
C. Fe(OH)3+3HCl=FeCl3+3H2O D. 2Fe2O3+3C 4Fe+3CO2↑
4Fe+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应方程式正确的是()
A. 2Na+CuSO4═Cu+Na2SO4 B. 4Na+O2 2Na2O
2Na2O
C. 2KNO3+CuCl2═Cu(NO3)2+2KCl D. Cu+2AgNO3═Cu(NO3)2+2Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是()
A. 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
B. 稀硫酸与氢氧化钡溶液混合:SO42﹣+Ba2+=BaSO4↓
C. 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O
D. 盐酸与澄清石灰水反应:H++OH﹣═H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 1 mol H2O的质量为18 g•mol﹣1
B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子的质量为32g
D. 标准状况下,1 molCCl4的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏德罗常数,下列叙述正确的是()
A. 标准状况下,22.4L H2O含有的分子数为1NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
C. 通常状况下,1NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于晶体说法的正确组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2﹣紧邻
⑥60gSi02中含Si﹣O键的个数为2NA
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
⑨124g P4含有P﹣P键的个数为4NA.

|
| A. | ①②③⑥ | B. | ①②④ | C. | ③⑤⑦ | D. | ③⑤⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com