
在无色透明的溶液中,能大量共存的离子组是( )
A.Na+、Mg2+、NO3-、CO32- B.K+、Cl—、NO3-、Fe2+
C.NH4+、Al3+ 、NO3-、SO42- D.H+、Na+、HCO3-、NO3-
、NO3-、SO42- D.H+、Na+、HCO3-、NO3-
科目:高中化学 来源: 题型:选择题
| A. | 正极质量不变 | B. | 电流通过导线由铜片流向银片 | ||
| C. | 烧杯中Ag+浓度逐渐减小 | D. | 电池工作时,铜片失电子,被还原 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上第一次月考化学卷(解析版) 题型:选择题
一定物质的量浓度的NaCl、MgCl2、AlCl3三种溶液与同体积同浓度的AgNO3完全反应,消耗三溶液的体积比为3:2:1,则三种溶液中Cl-的物质的量浓度之比为
A.1:1:1 B.1:2:3 C.3:2:1 D.2:3:6
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高一上10月月考化学试卷(解析版) 题型:选择题
VmL密度为ρg/mL的某溶液,含有相对分子质量为M的溶质mg,该溶液中溶质的质量分数为w%,物质的量浓 度为cmol/L那么下列关系式正确的是( )
度为cmol/L那么下列关系式正确的是( )
A.m=(VρW)/1000 B.c=(1000ρW)/M C.W%=[cM/(10ρ)]% D.C=m/(VM)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高一上10月月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
B.饱和石灰水跟盐酸反应:H++OH-═H2O
C.在硫酸溶液中加入氢氧化钡溶液:Ba2++OH-+ H++ SO42-═BaSO4↓+H2O
D.碳酸钙中加入盐酸:CO32-+2H+═CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:实验题
硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:
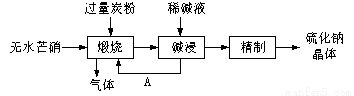
(1)上述流程中“碱浸”后,物质A必须经过 (填写操作名称)处理后,方可“煅烧”;若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为 。
(2)上述流程中采用稀碱液比用热水更好,理由是稀碱液能 Na2S水解(选促进或抑制)
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)= mol·L-1。(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
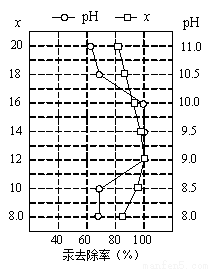
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如右图所示)。为使除汞效果最佳,应控制的条件是x控制 、pH控制 。
②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有 。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:选择题
下列有关实验原理、方法和结论都正确的是
A.向苯酚钠溶液中通入少量CO2,产物为苯酚和Na2CO3
B.向蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀,说明浓硫酸具有脱水性和强氧化性
C.将溴丙烷与足量氢氧化钠溶液混合加热,冷却后加硝酸银溶液,可检验溴元素
D.分别测定0.5 mol·L-1 H3PO4和H2SO4溶液的pH,比较磷和硫元素非金属性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
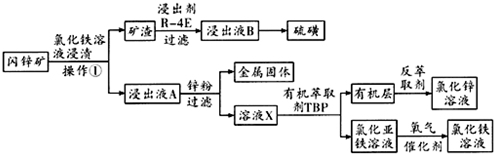
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com