
A.¢Ł¢Ś¢Ū B.¢Ü¢Ž C.¢Ś¢Ü¢Ż D.¢Ś¢Ż

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø13·Ö£©
£Ø1£© ÓĆNH3×öÖ÷ŅŖŌĮĻ°“ĻĀĮŠĮ÷³ĢÉś²ś»Æ·ŹNH4NO3”£ĘäÖŠ£į%”¢£ā%”¢£ć%·Ö±š±ķŹ¾¶ŌÓ¦·“Ó¦µÄ×Ŗ»ÆĀŹ£¬NH3ÓėHNO3·“Ӧɜ³ÉNH4NO3ŌĮĻĄūÓĆĀŹĪŖ100%
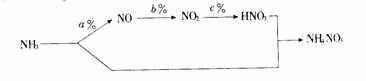
ČōÓĆ1£ōNH3ĪŖŌĮĻ£¬ĪŖĮĖŹ¹ÖʵƵÄNH4NO3²śĮæ×ī“ó£¬ŌņÓĆÓŚÖĘHNO3µÄNH3ÖŹĮæĪŖ””””””£ō£ØÓĆŗ¬£į”¢£ā”¢£ćµÄ“śŹżŹ½±ķŹ¾£©
£Ø2£© ļ§Ģ¬µŖ·ŹŌŚ¼īŠŌĢõ¼žĻĀŹ¹ÓĆ»įµ¼ÖĀ·ŹŠ§ĖšŹ§£¬NH4H2PO4ČÜŅŗÓė×ćĮæNaOHČÜŅŗ¹²ČČ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø3£© Ņ»ÖÖø“ŗĻ·ŹĮĻŗ¬ÓŠNH4NO3 ”¢NH4H2PO4”¢KCl£¬Č”ĘäŅ»¶ØĮæČÜÓŚĖ®ŠĪ³ÉČÜŅŗ£¬²āµĆĘäÖŠ²æ·ÖĄė×ÓÅضČĪŖ£ŗ£ć(NH4+)=3mol•l-1£¬£ć(H2PO4-)=2mol•l-1£¬£ć(K+)=2mol•l-1£¬ŌņÅäÖĘøĆø“ŗĻ·ŹĮĻĖłČ”µÄNH4NO3 ”¢NH4H2PO4”¢KClµÄĪļÖŹµÄĮæÖ®±ČĪŖ ”£
£Ø4£© ČĖĆĒŅ»Ö±ÖĀĮ¦ÓŚČĖ¹¤¹ĢµŖµÄŃŠ¾æŅŌ»ńµĆĮ®¼ŪµÄµŖ·Ź”£æĘѧ¼ŅĻČŗóĢį³ö²¢ŗĻ³É¹ĢµŖĆøµÄ¶ąÖÖÄ£ÄāĪļ”£ĘäÖŠŅ»ĄąŹĒŗ¬Mo”¢Fe”¢SŌ×ӵĔ°ĄąĮ¢·½Ģå”±½į¹¹£¬ČēĶ¼ĖłŹ¾£ŗ
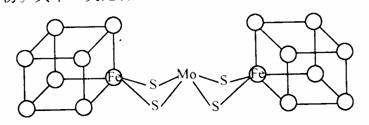
Ķ¼ÖŠ×ó”¢ÓŅĮ½±ß¶Ō³Ę£¬ø÷ŗ¬Ņ»øö½üĖĘĪŖĮ¢·½ĢåµÄ½į¹¹”£ĆæøöĮ¢·½Ģåŗ¬ÓŠ4øöFeŌ×Ó”¢4øöSŌ×Ó£¬ĖüĆĒĪ»ÓŚĮ¢·½ĢåµÄ8øö¶„µć£¬ĒŅŌ×Ó¼äÖ»ÓŠŅ»ÖÖ»Æѧ¼ü”£
¢ŁĒėŌŚĶ¼ÖŠ×ó±ßĮ¢·½ĢåµÄ”šÖŠĢīŠ“³öĘäÓą3øöFeŌ×Ó”£
¢ŚÉĻŹöŅ»øöĮ¢·½ĢåÖŠ4øöFeŌ×ÓĖłŌŚµÄ¶„µćĮ¬½ÓĖł¹¹³ÉµÄæÕ¼ä¼øŗĪĢåĪŖ ”””” ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com