

| A.CuFeS2仅作还原剂 |
| B.若有1molO2参加反应,则反应中有4mol电子转移 |
| C.方框中的物质应是CuS |
| D.SO2既是氧化产物,又是还原产物 |
科目:高中化学 来源:江苏 题型:单选题
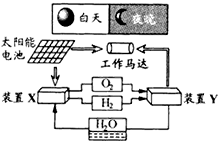
| A.该系统中只存在3种形式的能量转化 |
| B.装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:松江区二模 题型:单选题
| A.上述反应的生成物都是无毒的,所以燃放爆竹时不会污染环境 |
| B.该反应的发生需要点燃或撞击,所以它是一个吸热反应 |
| C.硫磺在黑火药爆炸的反应中既是氧化剂,又是还原剂 |
| D.KNO3有强氧化性,乘坐汽车、火车、飞机时不能随身携带 |
查看答案和解析>>
科目:高中化学 来源:浦东新区二模 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有硫酸铜作氧化剂 | ||
| B.SO42-既不是氧化产物又不是还原产物 | ||
| C.被氧化的硫与被还原的硫的质量比为3:7 | ||
D.1mol硫酸铜可以氧化
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.每生成1molFe3O4转移4mol电子 |
| B.该反应中Fe2+和S2O32-都是还原剂 |
| C.3molFe2+被氧化时有1molO2被还原 |
| D.反应方程式中化学计量数x=4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:吉林模拟 题型:单选题
| 序号 | 氧化剂 | 还原剂 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | FeCl3 | |
| ② | KMnO4 | H2O2 | O2 | MnO2 |
| ③ | KClO3 | 浓盐酸 | Cl2 | |
| ④ | KMnO4 | 浓盐酸 | Cl2 | MnCl2 |
| A.表中①反应的氧化产物只能有FeCl3 |
| B.表中②生成1mol的O2将有4mol的电子转移 |
| C.表中④的离子方程式配平后,H+的化学计量数为16 |
| D.表中③还原产物是KCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com