
| A. | C(s)+O2(g)=CO2(g)△H=+110.5 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.31 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol | |
| D. | 2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l)△H=-11036 kJ/mol |
分析 燃烧热是1mol可燃物完全燃烧生成稳定氧化物所放出的热量,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物,即碳元素变为二氧化碳,硫元素变为二氧化硫,氢元素变为液态水,据此分析.
解答 解:A、CO的化学计量数为1,产物为稳定氧化物,但碳的燃烧为放热反应,△H应为负值,故A错误;
B、甲烷的化学计量数为1,产物也是稳定氧化物,故△H代表燃烧热,故B正确;
C、H2的化学计量数为1,但产物不是稳定氧化物,生成的水应为液态,故△H不代表燃烧热,故C错误;
D、C8H18的化学计量数为2,△H不代表燃烧热,故D错误;
故选B.
点评 本题考察了燃烧热的概念.表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物,碳形成二氧化碳、氢形成液态水.


科目:高中化学 来源: 题型:解答题
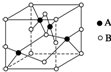 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):
实验室有一份混有碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,铝遇冷浓硝酸钝化 | B. | 浓盐酸的质量减轻 | ||
| C. | 澄清的石灰水变浑浊 | D. | 氢氧化钠固体发生潮解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度时,化学反应速率无论用A、C何种物质表示,其数值都是相同的 | |
| B. | 其他条件不变时,升高温度,反应速率加快 | |
| C. | 其他条件不变时,增大压强,反应速率加快 | |
| D. | 若增加或减少A的物质的量,反应速率一定会发生明显的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 11 | C. | 10 | D. | 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol任何气体的体积都约是22.4 L | |
| B. | 18 g NH4+含有电子数为10NA | |
| C. | NA个H2SO4分子的质量等于H3PO4的摩尔质量 | |
| D. | 标准状况下,相同体积的O2、HCl含有的分子数都为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com