
某研究小组通过实验探究Cu及其化合物的性质,下列操作正确且能达到目的的是
A.将铜丝插入浓硫酸中加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿
科目:高中化学 来源: 题型:
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾 溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
A.只有①④ B.只有③
C.只有②③ D.只有①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
胡椒酚是植物挥发油的成分之一,它的结构简式为:HO— —CH2CH=CH2,下列叙述中不正确的是( )
—CH2CH=CH2,下列叙述中不正确的是( )
A.1mol胡椒酚最多可与4molH2发生反应
B.1mol胡椒酚最多可与4mol溴发生反应
C.胡椒酚可与甲醛发生反应,生成聚合物
D.胡椒酚在水中的溶解度小于苯酚在水中的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在实验室合成了一种物质A。
⑴经分析,A的相对分子质量不超过100,A中C、H的质量分数分别为:
w(C)=69.76%,w(H)=11.63%,且完全燃烧后产物只有CO2和H2O。
则A的摩尔质量为 __________ 。
⑵ A的核磁共振氢谱如下图所示,且A可以和金属钠反应生成H2,但不能在Cu作催化剂下被催化氧化。(提示:羟基与碳碳双键相连的结构不稳定)
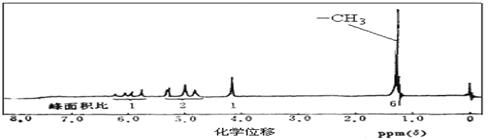
请根据以上信息写出A的结构简式 。
(3)A的某种同分异构体B分子中不含支链,能发生银镜反应。
请写出B发生银镜反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验设计能够达到目的的是
| 编号 | 实验目的 | 实验设计 |
| A | 证明盐酸酸性比醋酸强 | 用同一电路测等体积盐酸、醋酸溶液的导电性 |
| B | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| C | 证明钠的金属活动性比铜强 | 向CuCl2溶液中投入金属钠 |
| D | 证明溶液中含有I- | 向溶液中加入淀粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
同学们在做铜与浓硝酸反应的实验时,发现反应后溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确,这些方案中不可行的是
A.加水稀释该绿色溶液,观察颜色变化
B.加热该绿色溶液,观察颜色变化
C.向该绿色溶液中通入氮气,观察颜色变化
D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察溶液颜色变化
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化镁在医药、建筑等行业应用广泛。硫酸 镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
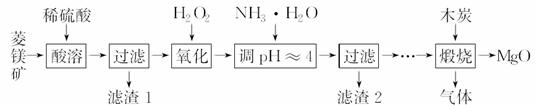
(1)MgCO3与稀硫酸反应的离子方程式为__________________________________。
(2)加入H2O2氧化时,发生反应的化学方程式为____________________________。
(3)滤渣2的成分是________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C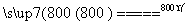 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体可以是________(填化学式)。
②B中盛放的溶液可以是________(填字母)。
a.NaOH溶液 b.Na2CO3溶液
c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用X射线对BaSO4穿透能力较差的特性,医学上在进行消化系统的X射线透视时,常用BaSO4作内服造影剂,这种检查手段称为钡餐透视。
(1)医学上进行钡餐透视时为什么不用BaCO3?(用离子方程式表示)________________________________________________________________________。
(2)某课外活动小组为了探究BaSO4的溶解度,分别将足量BaSO4放入:
a.5 mL 水;
b.40 mL 0.2 mol/L 的Ba(OH)2溶液;
c.20 mL 0.5 mol/L的Na2SO4 溶液;
d.40 mL 0.1 mol/L 的H2SO4 溶液中,溶解至饱和。
①以上各溶液中,Ba2+的浓度由大到小的顺序为________。
A.b>a>c>d B.b>a>d>c
C.a>d>c>b D.a>b>d>c
②已知298 K时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液b中的SO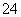 浓度为________ mol/L,溶液c中Ba2+的浓度为________ mol/L。
浓度为________ mol/L,溶液c中Ba2+的浓度为________ mol/L。
③某同学取同样体积的溶液b和溶液d直接混合,则混合液的pH为________(设混合溶液的体积为混合前两溶液的体积之和)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,可逆反应A(g)+3B(g) 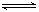 2C(g)达到平衡状态的标志是
2C(g)达到平衡状态的标志是
A. C生成的速率与A分解的速率2倍相等
B. 单位时间生成n mol A,同时生成3n mol B
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1∶3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com