
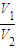 的取值范围是______.
的取值范围是______.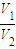 的值最小,假定为CO、O2的混合物,恰好反应,反应结束恢复原来的温度,反应后气体的体积V2最小,
的值最小,假定为CO、O2的混合物,恰好反应,反应结束恢复原来的温度,反应后气体的体积V2最小,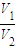 的值最大,据此解答.
的值最大,据此解答. 4CO2+6H2O(g)
4CO2+6H2O(g) aL
aL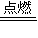 2CO2
2CO2 bL
bL aL+
aL+ bL=
bL=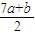 L,
L,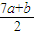 ;
; 4CO2+6H2O(g) 体积增大△V
4CO2+6H2O(g) 体积增大△V aL
aL 2CO2 体积减少△V′
2CO2 体积减少△V′ bL
bL aL=
aL= aL,故a:b=1:1,
aL,故a:b=1:1,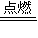 4CO2+6H2O(g)可知V(C2H6)=
4CO2+6H2O(g)可知V(C2H6)= V1,则:
V1,则: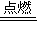 4CO2+6H2O(g) 体积增大△V
4CO2+6H2O(g) 体积增大△V V1
V1  V1
V1 V1=
V1=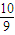 V1,故
V1,故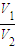 的极小值为
的极小值为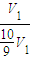 =0.9,
=0.9, 2CO2 可知V(CO)=
2CO2 可知V(CO)= V1,则:
V1,则: 2CO2 体积减少△V′
2CO2 体积减少△V′ V1bL
V1bL  V1L
V1L V1=
V1= V1,故
V1,故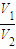 的极大值为V1109V1=1.5,
的极大值为V1109V1=1.5,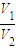 的取值范围是(0.9,1.5),
的取值范围是(0.9,1.5),

科目:高中化学 来源: 题型:
| 7a+b |
| 2 |
| 7a+b |
| 2 |
| V1 |
| V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.m>4 B.m=
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若H2的体积为
(2)若H2在混合气体中所占的体积分数为x,试计算当x为不同值时反应后总体积a的值(用x的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若a mL混合气体完全燃烧消耗相同条件下氧气的体积也为a mL(即V=a),则原混合气体中CH4的体积分数是____________。
(2)若完全燃烧后生成CO2和H2O(g)的总体积在相同条件下为2a mL,则原混合气体中CH4的体积分数是____________,现要测定原混合气体中H2的体积分数,还必须知道相同条件下的其他数据可以是____________(填选项)。
A.2a mL混合气体的密度 B.生成CO2的总体积 C.生成H2O(g)的总质量
(3)若原混合气体完全燃烧后的气体中只有CO2和H2O(g),则V的取值范围是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com