
分析 1g丙烷(C3H8)完全燃烧放热50.4kJ,则1molC3H8完全燃烧放热为50.4kJ×44=2217.6kJ,结合物质的状态、焓变书写热化学方程式.
解答 解:1g丙烷(C3H8)完全燃烧放热50.4kJ,则1molC3H8完全燃烧放热为50.4kJ×44=2217.6kJ,可知丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2217.6kJ/mol,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2217.6kJ/mol.
点评 本题考查热化学方程式的书写,为高频考点,把握反应中能量变化、焓变为解答的关键,侧重分析与应用能力的考查,注意物质的量与热量成正比,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
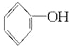 +2Na→2
+2Na→2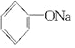 +H2↑
+H2↑ +3Br2→↓+3HBr
+3Br2→↓+3HBr +NaOH→
+NaOH→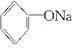 +H2O.
+H2O.| A. | ①和③ | B. | 只有② | C. | ②和③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌为负极,二氧化锰为正极 | |
| B. | 锌为正极,二氧化锰为负极 | |
| C. | 工作时电子由二氧化锰经外电路流向锌极 | |
| D. | 锌电极发生还原反应,二氧化锰发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
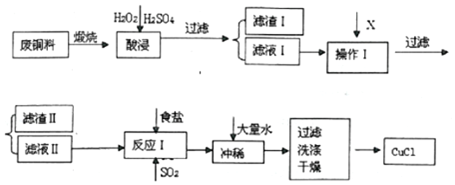
| 物质 | 开始沉淀pH | 沉淀完全pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.7 | 4.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| 1 | 2 | 3 | |
| 空白实验消耗硫酸铈标准溶液的体积(mL) | 0.75 | 0.50 | 0.80 |
| 0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.75 | 24.85 | 24.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 序号 | 加热前的质量 | 加热后的质量 | 失水质量 | 结晶水的值 | |
| m0(容器) | m1(容器+晶体) | m2(容器+无水硫酸铜) | |||
| 1 | 35.503g | 35.685g | 35.620g | ①0.065 | ②4.9 |
| 2 | 35.503g | 35.663g | 35.606g | ③0.057 | ④3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 铝箔在酒精灯上加热,熔化后的液态铝不滴落 | 高熔点的氧化铝薄膜兜在铝的外面,阻止了液态铝滴落 |
| B | 铁放在冷的浓硝酸中不溶解,无红棕色气体生成 | 铁遇浓硝酸钝化,表面形成致密的氧化膜,阻止内部铁继续与硝酸反应 |
| C | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| D | 将新制氯水滴到蓝色石蕊试纸上,试纸先变红后褪色 | 新制氯水中的H+使石蕊试纸先变红,HClO的强氧化性使石蕊试纸褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
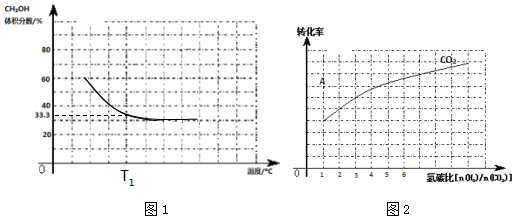
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝的化学性质稳定 | |
| B. | 铝在常温时与氧气不反应 | |
| C. | 铝具有金属性,也具有非金属性 | |
| D. | 铝与氧气反应生成一层致密的氧化物薄膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com