
【题目】下列能说明苯酚是弱酸的实验事实是
A. 苯酚遇FeCl3溶液呈紫色 B. 苯酚能与NaOH溶液反应
C. 常温下苯酚在水中的溶解度不大 D. 将CO2通入苯酚钠溶液出现浑浊
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种元素是短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W是该元素所在周期原子半径最大的元素,W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键,该分子中含有10个电子。Z原子最外层电子数是次外层电子数的3倍,试判断:
(1)X、Z两种元素的元素符号为X________,Z________。
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为________________。
(3)①由X、Y、Z所形成的常见离子化合物是__________________(写化学式)。
②该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为_______。
③化合物WY3的晶体结构中含有的化学键为________(选填序号)。
A.只含离子键 B.只含共价键 C.既含离子键又含共价键
④X与W形成的化合物与水反应生成X2,其中水作________(填“氧化剂”或“还原剂”)。
(4)用电子式表示化合物W2Z的形成过程:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某细胞中的含水量为:自由水∶结合水=90∶10,在水分总量不变的情况下,适当提高温度,则两种水的含量比值的变化是
A. 增大 B. 减小 C. 不变 D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A + B![]() 3C + 4D 反应中(各物质均为气体),表示该反应速率最快的是
3C + 4D 反应中(各物质均为气体),表示该反应速率最快的是
A. v(A)= 0.5 mol·L-1·s-1
B. v(B)= 0.3 mol·L-1·s-1
C. v(C)= 0.8 mol·L-1·s-1
D. v(D)= 30 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:

(1)该反应的化学方程式为______________________________;
(2)反应开始至2min,以气体Z表示的平均反应速率为__________;
(3)平衡时容器内混合气体密度比起始时________(填“变大”,“变小”或“相等”下同),混合气体的平均相对分子质量比起始时_________;
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________。
Ⅱ.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明I2(g)+H2(g)![]() 2HI(g)达到平衡状态的是_________。
2HI(g)达到平衡状态的是_________。
(2)一定能证明A(s)+2B(g)![]() C(g)+D(g)达到平衡状态的是________。
C(g)+D(g)达到平衡状态的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是
A. ![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
B. CH2=CH2+Br2 ![]() BrCH2CH2Br
BrCH2CH2Br
C. CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
D. CH3CH2CH2Br+NaOH![]() CH3CH2CH2OH+NaBr
CH3CH2CH2OH+NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔盐[(NH4)2Fe(SO4)2·8H2O]溶液经常用于定量滴定实验。下列有关说法正确的是
A. 配制0.1molL-1莫尔盐溶液500mL,需莫尔盐21.4克
B. 可与含HClO、H+、Clˉ微粒的溶液大量共存
C. 加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42-+Fe2++2OHˉ=2BaSO4↓+Fe(OH)2↓
D. 取样,加入浓NaOH溶液并加热,生成能使蓝色石蕊试纸变红的气体,证明含NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2000多年前,希腊生理学家和医学家希波克拉底发现,杨树、柳树的皮、叶中含有能镇痛和退热的物质。1800年,人们开始从该类植物中提取药物的活性成分——水杨酸(![]() )。1853年,德国化学家柯尔柏合成了水杨酸,并于1859年实现工业化生产。水杨酸虽然解热和镇痛效果很好,但由于酚羟基的存在,对肠道和胃粘膜有强烈的刺激,易引发呕吐和胃出血,而且味道令人生厌。1898年,德国化学家霍夫曼利用反应:
)。1853年,德国化学家柯尔柏合成了水杨酸,并于1859年实现工业化生产。水杨酸虽然解热和镇痛效果很好,但由于酚羟基的存在,对肠道和胃粘膜有强烈的刺激,易引发呕吐和胃出血,而且味道令人生厌。1898年,德国化学家霍夫曼利用反应:

制得乙酰水杨酸(阿司匹林),改善了水杨酸的疗效。1899年,由德国拜尔公司开始生产,并应用于临床,是第一种重要的人工合成药物。现代医药发展方向之一是合成药物长效化和低毒化,其有效途径是低分子药物高分子化,如:可将药物分子连在安全无毒的高分子链上。1982年,科学家通过乙二醇的桥梁作用把阿司匹林连接在高聚物上,制成缓释长效阿司匹林( ),用于关节炎和冠心病的辅助治疗。缓释长效阿司匹林分为高分子载体、低分子药物和作为桥梁作用的乙二醇三部分,在肠胃中水解变为阿司匹林,缓释长效阿司匹林使这种“古老”的解热镇痛药物重新焕发了“青春”。
),用于关节炎和冠心病的辅助治疗。缓释长效阿司匹林分为高分子载体、低分子药物和作为桥梁作用的乙二醇三部分,在肠胃中水解变为阿司匹林,缓释长效阿司匹林使这种“古老”的解热镇痛药物重新焕发了“青春”。
根据上述材料,结合所学知识,回答以下问题。
(1)水杨酸具有________和________的作用。
(2)霍夫曼制取阿司匹林的反应类型是________。
(3)在霍夫曼制取阿司匹林的反应中,可用于检验水杨酸是否完全反应的试剂是________。
(4)写出缓释阿司匹林在肠胃中水解出阿司匹林的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
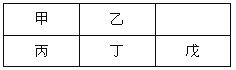
A. 原子半径:丙<丁<戊B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊D. 最外层电子数:甲>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com