
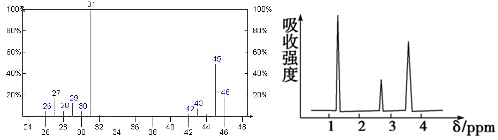
分析 根据元素守恒可判断有机化合物中一定含有C和H两种元素,根据生成8.8g的二氧化碳中C元素质量即为化合物中所含C元素质量、生成5.4g 的水中H元素质量即为化合物中所含H元素质量,对氧元素的确定要根据二氧化碳和水中的氧元素质量之和与氧气中氧元素的质量来分析,若前者大,则有机化合物有氧元素,两者相等,则有机化合物没有有氧元素,然后求出各自的物质的量,根据各元素的物质的量之比可推测最简式,根据具体C原子、H原子、O原子个数比判断;根据核磁共振氢谱表明其分子中有三种化学环境不同的氢原子来确定结构简式.
解答 解:根据质量守恒定律可知,化合物中所含C元素质量为:8.8g×$\frac{12}{44}$=2.4g,所含H元素质量为:5.4g×$\frac{2}{18}$=0.6g,二氧化碳和水中的氧元素质量之和为 (8.8g-2.4g)+(5.4g-0.6g)=11.2g,而氧气的质量为:$\frac{6.72L}{22.4L/mol}$×32g/mol=9.6g,所以有机物中氧元素质量为11.2g-9.6g=1.6g,n(C):n(H):n(O)=$\frac{2.4}{12}$:$\frac{0.6}{1}$:$\frac{1.6}{16}$=2:6:1,所以化合物的最简式是C2H6O,
在最简式C2H6O中,C、H原子已经达到饱和,其实验式即为分子式;
分子式为C2H6O,甲醚中只含一种H,由核磁共振氢谱表明其分子中有三种化学环境不同的氢原子,强度之比为3:2:1,为乙醇结构简式为:CH3CH2OH,
故答案为:C2H6O;否;CH3CH2OH.
点评 本题考查了有机物分子式、结构简式的确定,题目难度不大,明确常见有机物组成、结构与性质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:选择题
| A. | 煤和石油燃烧不完全时可排放出大量烟尘和CO | |
| B. | 化石燃料燃烧排出废气中含SO2,直接排到大气中会污染空气并形成酸雨 | |
| C. | 可通过物理方法把化石燃料转化为洁净燃料 | |
| D. | 氢能、核能、太阳能等都属于洁净、高效的新能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
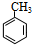 +HO-NO2$→_{△}^{浓H_{2}SO_{4}}$
+HO-NO2$→_{△}^{浓H_{2}SO_{4}}$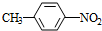 +H2O.
+H2O.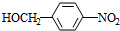 +
+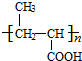 $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +nH2O.
+nH2O.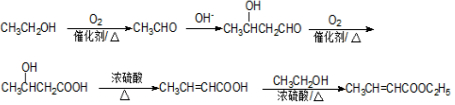 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lmol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| B. | 苯的结构简式为 ,能使酸性高锰酸钾溶液褪色 ,能使酸性高锰酸钾溶液褪色 | |
| C. | 相同物质的量的乙烯与乙醇分别在足量的O2中完全燃烧,消耗O2的物质的量相同 | |
| D. | 乙烯和植物油都能使溴水褪色,其褪色原理不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com