
【题目】金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞共用。金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量(单位:g·mol-1)。
(1)金晶体每个晶胞中含有________个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定_________。
(3)一个晶胞的体积为________cm3。
(4)金晶体的密度为________g·cm-3。
【答案】4 在立方体各个面的对角线上的3个金原子紧密排列且相邻的两个金原子处于相切状态 ![]()
![]()
【解析】
根据晶胞的概念及结构特点分析解答。
(1) 根据均摊法可计算金晶体每个晶胞中金原子数为8×![]() +6×
+6×![]() =4,所以金晶体每个晶胞中含有4个金原子,
=4,所以金晶体每个晶胞中含有4个金原子,
故答案为:4;
(2) 计算一个晶胞的体积,先要计算晶胞的边长,而晶胞的边长的大小与金原子的排列距离有关,所以除假定金原子是刚性小球外,还应假定在晶胞的面上对角线上的原子与原子要相切,
故答案为:在立方体各个面的对角线上的3个金原子紧密排列且相邻的两个金原子处于相切状态;
(3) 根据晶胞的结构可知,晶胞的对角线长为2d,所以晶胞的边长为![]() =
=![]() dcm,晶胞的体积为:(
dcm,晶胞的体积为:(![]() d)3=2
d)3=2![]() d3cm3,
d3cm3,
故答案为:2![]() d3;
d3;
(4)一个金晶胞中含有4个金原子,根据公式ρ=![]() =
=![]() =
=![]() g·cm-3;
g·cm-3;
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VCB是锂离子电池的一-种添加剂,以环氧乙烷(EO)为原料制备VCB的一种合成路线如下:

下列说法错误的是
A.反应①的原子利用率为100%
B.②的反应类型为取代反应.
C.EO、EC的一氯代物种数相同
D.CIEC、VCB分子中所有原子均处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是一种高效、低毒的消毒剂。其一种生产工艺如图所示。下列说法正确的是
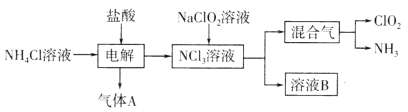
A.气体A为Cl2
B.参加反应的NaClO2和NCl3的物质的量之比为3:1
C.溶液B中含有大量的Na+、Cl-、OH-
D.可将混合气通过饱和食盐水除去C1O2中的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了如下装置制取和验证SO2的性质
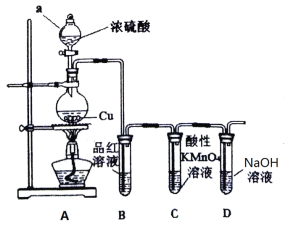
请回答:
(1)图中仪器a的名称为_____________。
(2)A中发生反应的化学方程式是_____________________________________。
(3)若C中溶液褪色,体现SO2具有_________________性。
(4)过量NaOH溶液与SO2反应的离子方程式是__________________________________。
(5)向两支装有品红溶液的试管中,分别通入Cl2和SO2,发现两支试管中品红溶液均褪色,请你设计实验证明哪支试管中通入的是SO2:_________________。
(6)该小组继续设计实验,相同条件下将Cl2和SO2两种气体按体积1:1混合,再通入品红溶液中,观察溶液几乎不褪色。查阅资料知:两种气体按体积1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组推测,某无色溶液中可能含有以下离子:K+、Al3+、Mg2+、Cu2+、NH4+、Cl-、CO32-、SO42-,进行如下实验:
①取适量该溶液,加入过量NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝色的气体,并得到澄清溶液。
②在①所得溶液中通入过量CO2,生成白色沉淀。
③另取原溶液于试管中,加足量BaCl2溶液后,得白色沉淀,再加稀盐酸,沉淀不溶解。
根据上述实验回答:
(1)写出①中反应生成气体的离子方程式_______________________________。
(2)该溶液中一定存在的离子有_____________,不能确定是否存在的离子有___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED系列产品是被看好的一类节能新产品,下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是
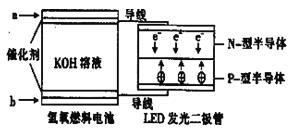
A.a处通入氢气,发生了还原反应:H2-2e-+2OH-=2H2O
B.b处通入氧气,为电池的正极
C.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替
D.P-型半导体连接的是电池负极.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,3.4 g NH3 的()
A.分子数约为 6.02×1023B.物质的量为 0.1 mol
C.体积约为 4.48 LD.氢原子的物质的量为 0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,G为电流计。有关的反应装置及部分反应现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小、b极质量增加 | 溶液中的SO42-向b极移动 | d极溶解c极有气体产生 | 电子从d极流向a极 |
由此可判断这四种金属的活动性顺序是
A. d>a>b>cB. a>b>c>dC. b>c>d>aD. a>b>d>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com