
分析 (1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO2系数为2,Cl2系数为1;再结合元素守恒,配平各物质的系数;
(2)根据HCl中氯元素化合价由-1价升高为Cl2中0价可知,HCl中氯元素被氧化,HCl在反应中还原剂与酸的作用,各占一半.
(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由-1价升高为Cl2中0价,据此计算转移电子物质的量;
(4)含元素化合价降低的物质为氧化剂,对应还原产物,含元素化合价升高的物质为还原剂,对应氧化产物.
解答 解:(1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由-1价升高为Cl2中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO2系数为2,Cl2系数为1;所以KClO3系数为2,KCl系数为2,HCl系数为4,水的系数是2,配平后的化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O,
故答案为:2;4;2;1;2;2;
(2)反应2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O中,HCl中氯元素化合价由-1价升高为Cl2中0价可知,HCl中氯元素被氧化,HCl在反应中还原剂与酸的作用,各占一半,
故答案为:②;
(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由-1价升高为Cl2中0价,所以产生0.1molCl2,转移的电子的物质的量为0.1mol×2=0.2mol,
故答案为:0.2;
(4)KClO3中氯元素化合价,为氧化剂,对应ClO2为还原产物,HCl中Cl元素的化合价升高为还原剂,对应的Cl2为氧化产物,
故答案为:KClO3;HCl;Cl2;ClO2.
点评 本题考查氧化还原反应,为高频考点,题目难度中等,把握反应中元素的化合价变化为解答的关键,注意掌握氧化还原反应的配平方法,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 还原剂是HCl,氧化剂是MnO2 | |
| B. | 每生成1 mol Cl2,转移电子的物质的量为2 mol | |
| C. | 每消耗1 mol MnO2,起还原剂作用的HCl消耗4 mol | |
| D. | 转移电子的物质的量为1 mol时,生成标准状况下Cl2的体积为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯应用液溴、铁屑和苯混合,反应后先用水再用稀碱液洗涤 | |
| B. | 检验C2H5Cl中氯原子,将C2H5Cl和NaOH溶液混合加热后,加稀硫酸进行酸化 | |
| C. | 用无水乙醇和浓H2SO4共热至140℃可以制得乙烯气体 | |
| D. | 苯酚中滴加少量的稀溴水出现了三溴苯酚的白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
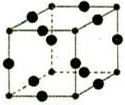 Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水不可用于鉴别苯、四氯化碳、乙醇三种无色液体 | |
| B. | 欲从溴水中分离出Br2,可将适量CCl4加入溴水中振荡静置分层后分液 | |
| C. | 配制一定物质的量浓度的硫酸溶液时,只需使用1次玻璃棒 | |
| D. | 氢气还原氧化铜实验先加热后通氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N×10-2 mol/L | B. | $\frac{N}{1.204×1022}$ mol/L | ||
| C. | $\frac{N}{6.02×1021}$mol/L | D. | $\frac{N}{6.02×1025}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体通入NaClO溶液中,若生成HClO,则可证明HClO是弱酸 | |
| B. | 高温下SiO2与碳酸盐反应,若生成CO2气体,则说明硅酸的酸性比碳酸强 | |
| C. | 向已配制的FeSO4溶液中加入2至3滴KSCN溶液,若溶液呈血红色,则说明可能有部分Fe2+被氧化为Fe3+ | |
| D. | 将铜片与浓硫酸混和共热,片刻后停止加热,冷却后再将溶液小心倒入盛有蒸馏水的烧杯中,若溶液呈蓝色,则说明铜能被浓硫酸氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com