
����Ŀ������ˮ�������ӵIJⶨ�����彡������Ҫ���壬ʵ���ҳ���Ī�����ⶨˮ���������Ӻ�����ʵ��������£���ˮ���м���K2CrO4 (��ɫ) ��Һ��ָʾ������AgNO3��Һ�ζ����յ㡣��֪��Ag2CrO4Ϊ������ˮ��ש��ɫ������������Ksp(AgCl)=1.8��10-10��Ksp(Ag2CrO4)= 1.8��10-12��
�ش��������⣺
��1���ζ�ʱ��Ӧʹ��____________(���ʽ����ʽ��) �ζ��ܣ�ԭ����_______________________��
��2��ˮ��Ӧ�������Ի������ԣ�ǿ����ʱ����K2CrO4��Һ������Ӧ�����ӷ���ʽ��___________________________________________��
��3���ζ��ﵽ�յ�ı�־��___________________________________________��
��4��ʵ������в���������±���
��� | 1 | 2 | 3 |
V(ˮ��)/mL | 10.00 | 10.00 | 10.00 |
c(AgNO3)/ mol��L-1 | 0.0010 | ||
V(AgNO3)/mL | 3.75 | 4.01 | 3.99 |
����ˮ���������ӵĺ���Ϊ_______________mg/L������2λС����
��5���������
�ٵ���Һ�еIJ���c(Cl-)=1.8��10-5mol/L�����ʱ��Һ��c(CrO42-)=____________��
����֪2AgCl+ CrO42-![]() 2Cl-+Ag2CrO4��������÷�Ӧ��ƽ�ⳣ��Ϊ____________��
2Cl-+Ag2CrO4��������÷�Ӧ��ƽ�ⳣ��Ϊ____________��
��6��������������ʵ��ⶨ���ƫ�͵���____________�������ţ�
A.��ƿϴ�Ӻ�δ����
B.�ζ�ǰ��δʹ�ñ�Һ��ϴ�ζ���
C.��ʽ�ζ��ܵζ�ǰ���Ӷ������ζ����Ӷ���
D.��ʽ�ζ��ܵζ�ǰ���첿�ֳ�����Һ���ζ�����ʱ�ζ��ܼ���������
���𰸡� ��ʽ AgNO3��Һˮ������� CrO 42-+2H+![]() Cr2O72-+H2O �μ����һ��AgNO3��Һʱ����ɫ���������ǣ�ǡ�ñ��ש��ɫ���Ұ���Ӳ����ԭɫ 14.20 1.8��10-2mol/L 1.8��10-8 CD
Cr2O72-+H2O �μ����һ��AgNO3��Һʱ����ɫ���������ǣ�ǡ�ñ��ש��ɫ���Ұ���Ӳ����ԭɫ 14.20 1.8��10-2mol/L 1.8��10-8 CD
����������1��AgNO3Ϊǿ�������Σ�ˮ��ʹ��Һ�����ԣ�����ʢ������ʽ�ζ����С��ʴ�Ϊ����ʽ����������Һˮ������ԡ�
��2��K2CrO4��H+�ᷢ�����淴Ӧ��CrO 42-+2H+![]() Cr2O72-+H2O������ˮ��Ӧ�������Ի������ԡ�
Cr2O72-+H2O������ˮ��Ӧ�������Ի������ԡ�
��3����Cl-ǡ�ó�����ȫʱ���ٵμ�һ����������Һ��Ag+ ��CrO 42-����Ag2CrO4��������ɫ�������ש��ɫ��������30s�ڲ���ɫ���ʴ�Ϊ���μ����һ��AgNO3��Һʱ����ɫ���������ǣ�ǡ�ñ��ש��ɫ���Ұ���Ӳ����ԭɫ��
��4����1����������Һ������������2��͵�3����ȣ����ϴ���ȥ��1�����ݣ��õ�2��͵�3�����ݵ�ƽ��ֵ���㡣���ĵ���������Һ�������ƽ��ֵΪ��3.99+4.01����10-3L/2=4��10-3L��n(Cl-)=n(Ag+)=4��10-3L��0.001 mol/L=4��10-6mol��m(Cl-)=4��10-6��35.5��103mg=142��10-3mg��ˮ���������ӵĺ���Ϊ142��10-3mg����10��10-3L��=14.20 mg/L��
��5����Ag+Ũ����ȣ�����c(Cl-)��c(Ag +)=1.8��10-10��c(CrO42-)��c2(Ag +)= 1.8��10-12 �����c(CrO42-)=1.8��10-2mol/L�� �ڶ���2AgCl+ CrO42-![]() 2Cl-+Ag2CrO4��ƽ�ⳣ��K=c2(Cl-)/c(CrO42-)= c2(Cl-)��c2(Ag +)/c(CrO42-)��c2(Ag +)=[ Ksp(AgCl)]2/ Ksp(Ag2CrO4)= (1.8��10-10)2/��1.8��10-12��=1.8��10-10��
2Cl-+Ag2CrO4��ƽ�ⳣ��K=c2(Cl-)/c(CrO42-)= c2(Cl-)��c2(Ag +)/c(CrO42-)��c2(Ag +)=[ Ksp(AgCl)]2/ Ksp(Ag2CrO4)= (1.8��10-10)2/��1.8��10-12��=1.8��10-10��
��6��.��ƿϴ�Ӻ���Ҫ����Բⶨ�����Ӱ�죻�ζ�ǰ��δʹ�ñ�Һ��ϴ�ζ��ܣ���ҺŨ�ȱ�С�������ı�Һ���ƫ���ƫ����ʽ�ζ��ܵζ�ǰ���Ӷ������ζ����Ӷ��������¶���ƫС�����ƫ�ͣ���ʽ�ζ��ܵζ�ǰ���첿�ֳ�����Һ���ζ�����ʱ�ζ��ܼ��������ݣ��в���Һ��δ�ų������ı�Һ���ƫС�����ƫ�͡��������ʵ��ⶨ���ƫ�͵���CD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������,��Ԫ����H2A��Һ�еμ�NaOH��Һ,���û����ҺpH������Ũ�ȱ仯��ͼ��ʾ,����˵����ȷ���ǣ� ��

A. ֱ��M��ʾpH��lg![]() �ı仯��ϵ
�ı仯��ϵ
B. Ka2(H2A)=10-4.3
C. ����e����Һ�У�c(H2A)=c(A2-)>c(HA-)>c(H+)>c(OH-)
D. f����Һ�У�c(H+)-c(OH-)=c(HA-)+c(A2-)-c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������NaOH��������1.0 mol��L��1��NaOH��Һ240 mL��
(1)������Һʱ��һ����Է�Ϊ���¼������裺
�ٳ������ڼ��㡡���ܽ⡡��ҡ�ȡ���ת�ơ���ϴ�ӡ��߶��ݡ�����ȴ����ҡ��
����ȷ�IJ���˳��Ϊ__________________�������õ��IJ����������ձ�����ͷ�ιܡ�________________��
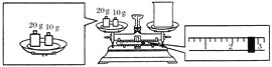
(2)ijͬѧ������NaOH��������������������ƽ�����ձ�����������ƽƽ����״̬��ͼ��ʾ���ձ���ʵ������Ϊ________ g��Ҫ��ɱ�ʵ���ͬѧӦ�Ƴ�________ g NaOH��
(3)ʹ������ƿǰ������е�һ��������________��
(4)��ͼ�Ǹ�ͬѧת����Һ��ʾ��ͼ��ͼ��������������д����
��________________________________________________________________________
��________________________________________________________________________
(5)�����ƹ����У���������������ȷ�ģ����в������������ƫ�ߵ���________(����ĸ)��
A������NaOH�Ѿ�����
B��������ƿ�м�ˮδ���̶���
C��������NaOH��Һ�������ձ���
D���ô������������ƽ��5.4 g NaOH(1 g����������)ʱ����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������¼Ƭ��֮�¡��е�PM2.5�ǿ�����Ⱦ��֮һ������PM2.5 ָ( )
A. �������� B. SO2 C. �������� D. CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��K2Cr2O7��һ����Ҫ�Ļ���ԭ�ϡ��Ը�����(��Ҫ�ɷ�ΪFeO��Cr2O3��������Al2O3��Fe2O3������)Ϊԭ���Ʊ�K2Cr2O7��һ�ֹ����������£�

��֪��
��4FeO��Cr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
��Cr2O72-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
��1����������ʱ��Al2O3��Na2CO3������Ӧ�Ļ�ѧ����ʽΪ___________��
��2��������������Ҫ�ɷ���________(�ѧʽ).
��3�����ữ�����������ҺpH<5����Ŀ����_________
��4����ת����һ��������Ӧ�Ļ�ѧ����ʽΪ____________
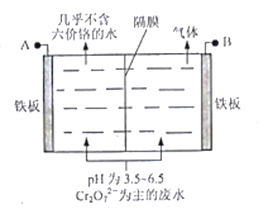
��5�����õ�ⷨ����������ˮԭ������ͼ��ʾ����������Һ�з�����Ӧ��Cr2O72-+6Fe2++14H+ == 2Cr3+ +6Fe3+ + 7H2O�������ĵ缫��ӦʽΪ_______����������������Ϊ_______(�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ���ڵ绯ѧ��Ӧ�ù㷺���ش��������⣺
��1�����ݷ�Ӧ2Fe3++Cu==2Fe2++Cu2+���ԭ�����ͼ����������ʾ��������Ϊ��a��b��

�ٵ缫BΪ____________���������ҺCΪ_____________�������ţ�
A,̼�� B.ͭƬ C.Fe2(SO4)3��Һ D.CUSO4��Һ
��A�缫�ĵ缫��ӦʽΪ________________________________________��
���øõ������Դ�������������Һ��������������11.2mL��������״��������ʱ���õ����__________________molFe3+����ԭ��
��2��NaFeO4��һ����;�㷺�Ļ�����Ʒ����ҵ�ϳ��õ�ⷨ��ȡ����ȡװ����ͼ����֪Na2FeO4ֻ��ǿ���������±Ƚ��ȶ�������ǿ�����ԡ�

��Na2FeO4����Ԫ�ػ��ϼ�Ϊ_____________ Na2FeO4�Ǿ���ɱ��Ч���ľ�ˮ����ԭ����_________________________________________________��
���缫NiΪ_________________������������������������Ϊʹ��װ���ܳ�����Ӧ�����ӽ���ĤӦΪ__________________________�����������������������ӽ���Ĥ��
��������ӦʽΪ_______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���������ȫ�����л������__________��ȫ����������__________��
A.CH4��C2H5OH��C6H12O6(����)��(C6H10O5)n(����)
B.C2H2��H2O2��CCl4��C6H6
C.CH4��C2H4��H2CO3��CH3Cl
D.CH4��C2H6��C2H2��C6H6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɽ������ķ�Ӧ�ѳ�Ϊ��Ҫ�ĺϳɹ��ߣ�������ɱ��ߣ���Ի�����ɵIJ���Ӱ�졣����о��ɱ������ĺ��̡������ܡ�����ͭ�ȴ���Ӧ�ó�Ϊ�ȵ����������Ժ��ܷ�������Ҫ�ɷ�CoO��Co2O3��������Al2O3��ZnO�����ʣ�Ϊԭ���Ʊ�CoCO3��һ�ֹ���������
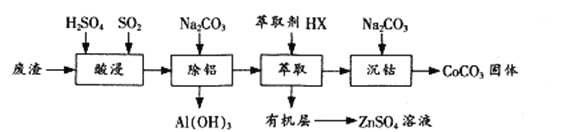
�±��г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0 mol/L���㣩
�������� | ��ʼ������pH | ������ȫ��pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
�ش��������⣺
��1���������ʱͨ��SO2��Ŀ���� ____________����Ӧ�����ӷ���ʽΪ______________��
��2������ȡ�����̿ɱ�ʾΪZnSO4��ˮ�㣩+2HX���л��㣩![]() ZnX2���л��㣩+H2SO4��ˮ�㣩�����л����ȡZnSO4��Һ�IJ����� __________________��
ZnX2���л��㣩+H2SO4��ˮ�㣩�����л����ȡZnSO4��Һ�IJ����� __________________��
��3�������ܡ�ʱNa2CO3��Һ�軺���μӵ�ԭ���� ____________��
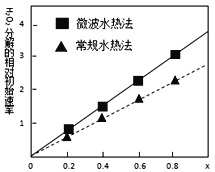
��4���õõ���CoCO3��Ϊԭ�ϲ�����ˮ�ȷ��ͳ���ˮ�ȷ������Ƶ�����CoxNi(1-x)Fe2O4������Co��Ni��Ϊ+2�ۣ�����������H2O2�ֽ�Ĵ������нϸߵĻ�������ͼ�����ֲ�ͬ�����Ƶõ�CoxNi(1-x)Fe2O4��10��ʱ���ֽ�6%��H2O2��Һ����Գ�ʼ������x�仯���ߡ���ͼ����Ϣ��֪��____________����ȡ�õ��Ĵ������Ը��ߣ��ɴ��Ʋ�Co2+��Ni2+���������д�Ч�����õ���____________ ��
��5���ô������ת����Ҳ���ԴӲ�����(CoC2O4)���ϵõ�CoCO3������CoC2O4�������Һ�еμ�Na2CO3��Һ������CoCO3��������ʱ����Һ��![]() =___________��[��֪Ksp(CoC2O4)=6.3��10-8 Ksp (CoCO3)=1.4��10- 13]
=___________��[��֪Ksp(CoC2O4)=6.3��10-8 Ksp (CoCO3)=1.4��10- 13]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����25mL 0.1000mo1��L-1 HA��Һ�μ�ͬŨ�ȵ�BOH��Һ�������ҺpH��μ�BOH��Һ�ı仯����ͼ��ʾ�������й������������
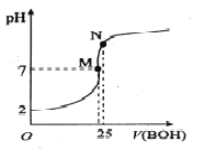
A. BA��Һ�ʼ���
B. ��HA�ĵ��볣��ԼΪ0.0011
C. M��ʱc(B+��=c(A-��> c(H+��= c(OH-��
D. N��ʱ����10mL0.1mol/L HA��Һ�����ٽ�A-��ˮ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com