
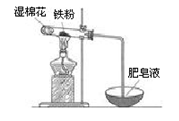
 Fe3O4 + 4H2 ② b
Fe3O4 + 4H2 ② b Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 3SO2 + 6H2O CO2 +2SO2 +2H2O
CO2 +2SO2 +2H2O  Fe3O4 + 4H2。
Fe3O4 + 4H2。 Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 3SO2 + 6H2O CO2 +2SO2 +2H2O。
CO2 +2SO2 +2H2O。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源:不详 题型:填空题
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.残余固体是铜和铁 |
| B.最后得到的溶液中一定含有Cu2+ |
| C.将残余固体加入到稀硫酸中,有气泡产生 |
| D.最后得到的溶液中可能含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
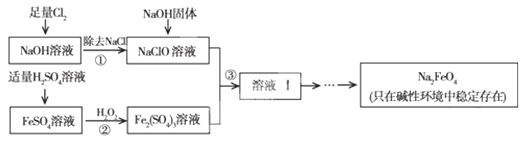
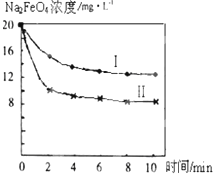
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
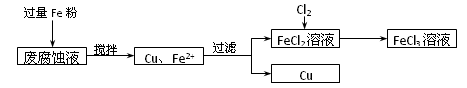

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入适量稀盐酸,微热。 | 黑色粉末逐渐溶解,有无色气体逸出。 |
| ② | 向试管1所得溶液中滴加几滴 KSCN溶液,振荡。 | 溶液未出现血红色 |
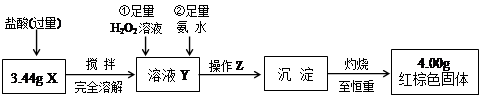

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2O3 | B.Fe3O4 | C.Fe4O3 | D.Fe5O7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com