
| A. | 它的最外层电子数为4 | B. | 它的金属性比铅强 | ||
| C. | 它的最高价氧化物的水化物是强酸 | D. | 它的位置在第7周期IVA族 |
分析 根据具有相当稳定性的同位素称为类铅,则114号是第7周期IVA族的元素,可以得到两个结论:一、属于碳族元素;二、在周期表中处于元素Pb的下方,根据元素周期律,同一主族,元素的性质具有相似性和递变性来解答.
解答 解:A.第7周期IVA族元素的最外层电子数均为4,故A正确;
B.同主族元素的原子,从上到下失电子能力逐渐增强,114号元素在周期表中处于元素Pb的下方,故它的失电子能力比铅强,故B正确;
C.该元素为金属元素,其最高价氧化物的水合物不可能是强酸,故C错误;
D.具有相当稳定性的同位素称为类铅,则114号是第7周期IVA族的元素,故D正确;
故选C.
点评 本题主要考查了同一主族元素的性质具有相似性和递变性这一知识,题目难度不大,熟悉元素周期律即可解答,注重知识的迁移应用来解答,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L HCl溶液中含有0.1NA个HCl分子 | |
| B. | 23gNa在空气中燃烧生成Na2O2时转移电子数目为2NA | |
| C. | 28gCO和N2的混合气体中电子数目为14NA | |
| D. | 11.2LCO2含氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的热稳定性:H20>NH3 | |
| B. | 最高价氧化物对应水化物的酸性:H3PO4<H2SO4 | |
| C. | 原子半径:Na>Mg>Al | |
| D. | N元素的最高价氧化物对应的水化物和它的氢化物反应不能生成盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物中不可能含有离子键 | |
| B. | 阴阳离子之间通过静电引力形成的化学键叫离子键 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最终可生成0.2 mol NH3 | |
| B. | 增大压强能使反应速率减小 | |
| C. | 降低反应体系的温度能加快反应速率 | |
| D. | 向容器中再加入N2,能加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池把氢气和氧气燃烧放出的热能转化为电能 | |
| B. | 电解水制取氢气是理想而经济的制氢方法 | |
| C. | 氢氧燃料电池汽车的使用可以有效减少城市空气污染 | |
| D. | 燃料电池的能量转化率可达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑥ | ⑦ | ⑨ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ④ |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 3a+b-c | B. | 3a-c+b | C. | a+b-c | D. | c-a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
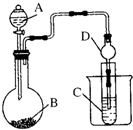
| A. | 仪器A的名称长颈漏斗,仪器 D的名称为球形干燥管 | |
| B. | 若利用上装置验证非金属性:Cl>S,装置A、B、C中所装药品应分别为稀盐酸、MnO2、Na2S溶液 | |
| C. | 若利用上装置证明非金属性:S>C>Si,装置A、B、C中所装药品应分别为稀硫酸、Na2CO3溶液、Na2SiO3溶液,观察到B中产生气泡,试管C中出现白色沉淀现象,则可以证明非金属性:S>C>Si | |
| D. | 装置A、B、C中所装药品应分别为稀盐酸、Na2CO3溶液、Na2SiO3溶液,观察到B中产生气泡,试管C中出现白色沉淀现象,则可以证明非金属性:Cl>C>Si |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com