
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | 混合溶液的pH值应等于7 | |
| B. | 如果酸是强酸,则pH一定小于7 | |
| C. | 如果碱是强碱,则pH一定不大于7 | |
| D. | 如果混合液的pH大于7,则碱一定为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 研发易降解的生物农药 | |
| B. | 对燃煤进行脱硫处理 | |
| C. | 对塑料等垃圾进行深埋或倾倒入海处理 | |
| D. | 推广使用节能环保材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向豆浆中加入盐卤做豆腐 | |
| B. | 钢笔使用不同牌子的墨水堵塞 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一束光亮的通路 | |
| D. | 向石灰水中通入二氧化碳气体产生白色浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
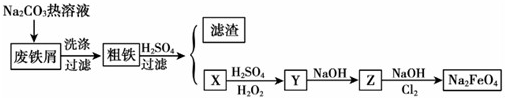
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主要原料:碳酸钙 食用方法:每日一次,每次一片,嚼食. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把没用完的药品倒回原试剂瓶中保存 | |
| B. | 配制稀硫酸时,先在量筒内放好水,再缓缓地加入一定量的浓硫酸 | |
| C. | 用天平称量药品质量时,先加质量大的砝码,再加质量小的砝码 | |
| D. | 用排水取气法收集气体时,导管应插入试管底部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com