
【题目】用化学用语表示:
(1)根据下列几种粒子的结构示意图,回答问题:

①写出B微粒的符号_________;
②若A微粒的中子数为10,写出表示A微粒的组成符号________;
③写出A、C、D三种元素形成的某种化合物在水溶液中的电离方程式:_________;
(2)写出下列反应的化学方程式:
①氯化铵与氢氧化钠共热____________;
②工业上制备氯气____________。
【答案】O2- ![]() 或18O Na2SO4= 2Na++SO42-或 Na2SO3= 2Na++SO32- NH4Cl+NaOH
或18O Na2SO4= 2Na++SO42-或 Na2SO3= 2Na++SO32- NH4Cl+NaOH![]() NaCl+NH3↑+H2O 2NaCl + 2H2O
NaCl+NH3↑+H2O 2NaCl + 2H2O![]() 2NaOH + Cl2↑+H2↑
2NaOH + Cl2↑+H2↑
【解析】
⑴①B为氧元素,由于核外电子数大于核内质子数,B为阴离子,B微粒的符号为O2-,故答案为:O2-;
②A为氧原子,质子数8,A微粒的中子数为10,A微粒的组成符号![]() 或18O,故答案为:
或18O,故答案为:![]() 或18O;
或18O;
③A、C、D对应的三种元素为O、S、Na,三种元素形成的某种化合物可能为Na2SO4或 Na2SO3,因此在水溶液中的电离方程式:Na2SO4= 2Na++SO42-或 Na2SO3= 2Na++SO32-,故答案为:Na2SO4= 2Na++SO42-或 Na2SO3= 2Na++SO32-;
⑵①氯化铵与氢氧化钠共热反应生成氯化钠、氨气和水,其反应方程式为NH4Cl+NaOH![]() NaCl+NH3↑+H2O,故答案为:NH4Cl+NaOH
NaCl+NH3↑+H2O,故答案为:NH4Cl+NaOH![]() NaCl+NH3↑+H2O;
NaCl+NH3↑+H2O;
②工业上制备氯气主要是电解饱和食盐水,其反应方程式为2NaCl + 2H2O ![]() 2NaOH + Cl2↑+H2↑,故答案为:2NaCl + 2H2O
2NaOH + Cl2↑+H2↑,故答案为:2NaCl + 2H2O![]() 2NaOH + Cl2↑+H2↑。
2NaOH + Cl2↑+H2↑。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. HClO、H2CO3、HNO3、HClO4的酸性依次增强
B. 苹果酸![]() 含有1个手性碳原子
含有1个手性碳原子
C. HCl、NH3、C2H5OH均易溶于水的原因之一是与H2O分子均形成氢键
D. 以极性键结合的分子不一定是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100molL﹣1 NaOH溶液分别滴定20.00mL 0.100molL﹣1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是( )
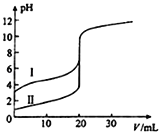
A. Ⅱ表示的是滴定醋酸的曲线
B. V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣)
C. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
D. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环与环之间共用两个或多个碳原子的多环烷烃称为桥环烷烃,其中二环[1.1.0]丁烷 (![]() )是其中一种。下列关于该化合物的说法正确的是
)是其中一种。下列关于该化合物的说法正确的是
A. 与C3H4是同系物
B. 一氯代物只有一种
C. 与环丁烯互为同分异构体
D. 所有碳原子可能都处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同。已知2NO+O2==2NO2,打开活塞,使NO与O2充分反应,则下列说法正确的是
A. 开始时左右两室分子数相同B. 反应开始后NO室压强增大
C. 最终容器内密度与原来相同D. 最终容器内仍然有NO剩余
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知亚硝酸钠能发生如下反应:2NaNO2+ 4HI= 2NO + I2 + 2NaI + 2H2O
(1)用双线桥表示电子转移的方向与数目__________。
(2)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为_________。
II.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O
(1)该反应中还原产物为__________。
(2)每生成2molCuI,有__________mol KI被IO3-氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。某化学兴趣小组设计如图装置以制备Cl2O(支撑及夹持装置已省略)。
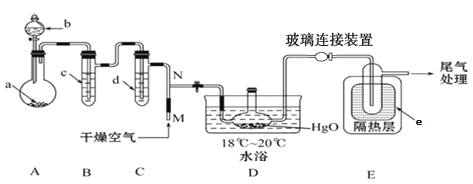
已知:① a中固体试剂是MnO2,b中试剂是浓盐酸。 ②Cl2O的部分性质如下表。
熔点 | 沸点 | 制备方法 |
-120.6 ℃ | 3.8℃ | 2HgO+2Cl2 = Cl2O+HgCl2·HgO |
请回答:
(1)指出该制备装置中存在的一个明显错误______________(经改进后进行有关实验)。
(2)装置C中盛有的试剂是______________。
(3)写出装置A中制备Cl2的化学方程式__________。
(4)装置D中采用18℃~20℃水浴的原因之一是如温度过低,反应速率慢,另一个可能的原因是 ___________。
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是____________。
(6)Cl2O是市场上一种比较理想的饮水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2消毒能力是等质量Cl2O的_________倍(结果保留两位小数)
(7)文献报道说,Cl2O的另一种制备方法是利用Cl2与足量的Na2CO3溶液反应来制得,写出该反应的化学方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制100mL 0.2 mol·L-1的Na2CO3溶液,试回答下列问题:
(1)若要实施配制,除天平、烧杯、玻璃棒外,还需的玻璃仪器有________, ________;
(2)配制完毕后,教师指出有三位同学进行了下列某一项错误操作,你认为这三项错误操作中会导致所得溶液浓度偏高的是________(填选项字母)
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度线
(3)通过计算得出可用天平称取Na2CO3固体________g。若用4 mol·L-1的Na2CO3浓溶液配制100 mL 0.2 mol·L-1的稀溶液,应用量筒量取______mL该浓溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图,回答问题。
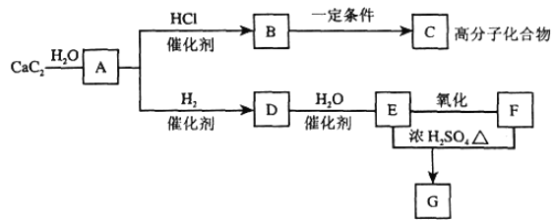
(1)有机物的结构简式:C._________________, E_______________。
(2)①反应DE的化学方程式是___________________________________________。
②E和F反应生成G的化学方程式是_______________,反应类型为__________。
③实验室制取A的化学方程式__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com