
 ��Ԫ�س����������ۣ�����������������������������������������������������ͬѧͬʱ���ʵ�鷽������֤���Ʋ��Ƿ���ȷ�������ʵ�鷽���������������������� ��
��Ԫ�س����������ۣ�����������������������������������������������������ͬѧͬʱ���ʵ�鷽������֤���Ʋ��Ƿ���ȷ�������ʵ�鷽���������������������� �� ���л��ϳɹ�ҵ��һ��ԭ�ϡ���ҵ������
���л��ϳɹ�ҵ��һ��ԭ�ϡ���ҵ������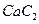 ��ˮ��Ӧ������Ȳ��
��ˮ��Ӧ������Ȳ��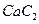 ��
�� ��
�� ��Ϊ�ȵ����壬
��Ϊ�ȵ����壬 �ĵ���ʽ��
�ĵ���ʽ�� ��ʾΪ ��1mol
��ʾΪ ��1mol  �к��е�
�к��е� ����ĿΪ_ ��
����ĿΪ_ ��
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��12��17 | B��13��10 | C��11��8 | D��8��16 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CaCl2 | B��H2O2 |
| C��Na2 O2 | D��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
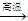 4FeO��CO2��Ϊ�Ƶ����ֻ�����ߵĴ�����Ӧ��480 g Fe2O3��ĩ�м���̿�۵�����Ϊ_____g��
4FeO��CO2��Ϊ�Ƶ����ֻ�����ߵĴ�����Ӧ��480 g Fe2O3��ĩ�м���̿�۵�����Ϊ_____g�� C(g) + D(g) ��H =" Q" kJ��mol��1
C(g) + D(g) ��H =" Q" kJ��mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ӧ��������������������������ʱ���÷�Ӧһ�����ܷ��� |
| B����ʯī�Ƚ��ʯ�ȶ���֪��C�����ʯ��s��=C��ʯī��s����H<0 |
C����֪��2SO2��g��+O2��g�� 2SO3��g����H=һ98��3kJ/mol����lmolSO2��0��5molO2 2SO3��g����H=һ98��3kJ/mol����lmolSO2��0��5molO2���� һ�ܱ������г�ַ�Ӧ���ų�49��15kJ������ |
| D����101kPa��25��ʱ��lgH2��ȫȼ��������̬ˮ���ų�120��9kJ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com