
分析 将22.85克MgCl2和AlCl3的混合物投入过量的NaOH溶液中,充分反应后得到5.8克沉淀,沉淀是氢氧化镁,根据镁守恒n(MgCl2)=n[Mg(OH)2]=$\frac{5.8}{58}$=0.1mol,则m(MgCl2)=0.1mol×95g/mol=9.5g,所以m(AlCl3)=22.85g-9.5g=13.35g,再结合n=$\frac{m}{M}$分析求解.
解答 解:将22.85克MgCl2和AlCl3的混合物投入过量的NaOH溶液中,充分反应后得到5.8克沉淀,沉淀是氢氧化镁,根据镁守恒n(MgCl2)=n[Mg(OH)2]=$\frac{5.8}{58}$=0.1mol,则m(MgCl2)=0.1mol×95g/mol=9.5g,所以m(AlCl3)=22.85g-9.5g=13.35g,n=$\frac{m}{M}$=$\frac{13.35g}{133.5g/mol}$=0.1mol,答:原混合物中AlCl3为0.1mol.
点评 本题考查混合物反应的计算,侧重考查学生分析解决问题能力,题目难度中等,利用守恒思想进行解答,可以简化计算过程,试题培养了学生的分析、理解能力及化学计算能力.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )| A. | II表示的是滴定醋酸的曲线 | |
| B. | V(NaOH)=20.00ml时,两份溶液中c(Cl-)=c(CH3COO-) | |
| C. | pH=7时,滴定醋酸消耗V(NaOH)小于20ml | |
| D. | V(NaOH)=10.00ml时,醋酸溶液中:2c(OH-)-2 c(H+ )=c(CH3COO-)-c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=C(CH3) CH3 3-甲基-2-丁烯 | |
| B. | CH3CH(CH3)CH(Cl)CH3 3-甲基-2-氯丁烷 | |
| C. | CH3CH(OH)CH2CH3 2-羟基丁醇 | |
| D. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5mol/L | B. | 3.0mol/L | C. | 2.0mol/L | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向NaClO溶液中滴入少量FeSO4溶液:2Fe2++ClO-+2H+=Cl-+2Fe3++H2O | |
| B. | 氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+3H2O | |
| C. | 碳酸氢钠溶液与少量澄清石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O | |
| D. | Na2SO3溶液中SO32-的水解:SO32-+H2O$\frac{\underline{\;电解\;}}{\;}$HSO3-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 陶瓷、水泥和光导纤维均属于硅酸盐材料 | |
| C. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 | |
| D. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
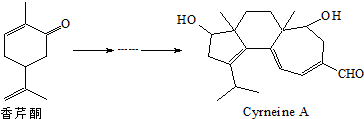
| A. | 香芹酮化学式为C9H12O | |
| B. | Cyrneine A可以发生加成反应、消去反应和氧化反应 | |
| C. | 香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色 | |
| D. | 香芹酮和Cyrneine A可以通过氯化铁溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (-R、-R′代表烃基或氢原子)
(-R、-R′代表烃基或氢原子) 的单体是CO2和
的单体是CO2和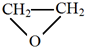 .
.
 ,名称是1,3-丁二烯.
,名称是1,3-丁二烯.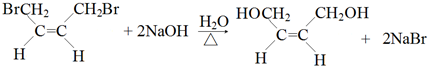 .
.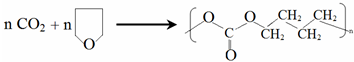 .
. .
. .
.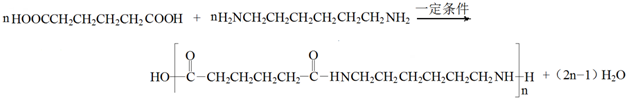 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com